ROTURA DEL LIGAMENTO CRUZADO ANTERIOR, UNA LESION DEPORTIVA DE LA RODILLA MUY FRECUENTE
16 abril 2022
Síndrome de espalda fallida: “la cirugía de espalda esta bien pero me sigue doliendo”.
16 marzo 2022
COMPLICACIONES QUIRURGICAS DE LA CIRUGÍA DE HERNIA DISCAL PARTE 2. (LESIONES VASCULARES )
17 febrero 2022
COMPLICACIONES QUIRURGICAS DE LA CIRUGÍA DE HERNIA DISCAL PARTE 1. (ROTURA DURAL, FISTULA DE LCR, DEFICIT NEUROLÓGICO, MENINGITIS, LESIÓN CEREBRAL)
17 enero 2022
En portada
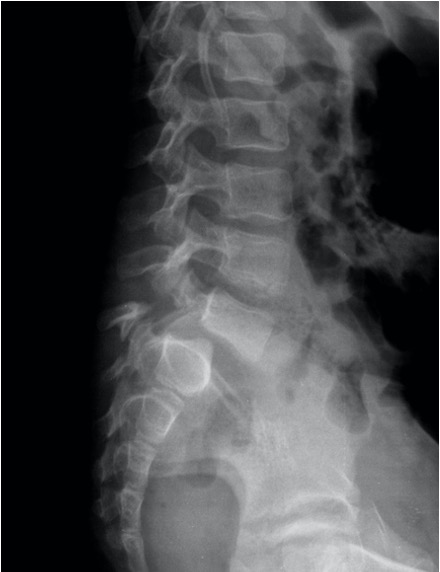
ESPONDILOLISTESIS Y ESPONDILOLISIS: UNA CASUSA DE DOLOR LUMBAR
20 agosto 2022El dolor lumbar es una de las principales causas de consulta en atención primaria y en traumatología. El 90% de las veces cede de forma espontánea y suele ser dolor muscular o tensional. En otras ocasiones este dolor permanece y hay causas raquídeas que los justifican como es la espondilolistesis o la espondilólisis. Explicamos todo sobre esta patología.
¿QUÉ ES LA ESPONDILOLISTESIS Y ESPONDILOLISTESIS?
El término espondilolistesis hace referencia al desplazamiento de una vértebra respecto a la vértebra adyacente inferior. El desplazamiento de la vértebra puede ser hacia una dirección posterior (retrolistesis), o bien hacia anterior (anterolistesis), que es lo más frecuente. La espondilólisis es la alteración o rotura del arco posterior de las vertebras pero a diferencia de la listesis no hay desplazamiento de una vertebra sobre ella. En ocasiones es el paso previo a la espondilolistesis. La incidencia de esta patología está entre el 3-10%. El lugar más afectado es L4 y L5.¿QUÉ TIPOS DE ESPONDILOLISTESIS HAY?
Existen varios tipos de espondilolistesis que se recogen en la siguiente clasificación etiopatogénica:- Tipo I o displásica: debida a un déficit o displasia congénita facetaria.
- Tipo II o ístmica: consecuencia de espondilólisis (fractura o elongación de la pars interarticularis).
- Tipo III o degenerativa: debida a la inestabilidad asociada a la cambios degenerativos.
- Tipo IV o traumática: consecuencia de traumatismos que no afectan a la pars interarticularis.
- Tipo V o patológica: asociada a enfermedades óseas (ej.: osteoporosis, Paget, metástasis).
- Tipo VI o posquirúrgico: producida por la pérdida de elementos óseos en una cirugía.
¿QUÉ GRADOS DE ESPONDILOLISTESIS HAY?
La escala de Meyerding permite clasificar el grado de desplazamiento en las radiografías laterales:- Grado I: <25%
- Grado II: 25-50%
- Grado III: 50-75%
- Grado IV: 75-100%
- Grado V: >100% o espondiloptosis (implica que la vertebra superior está desplazada sobre la vértebra inferior en toda su longitud, y, por tanto, se verticaliza por delante de la vértebra inferior)
CARACTERÍSTICAS Y MANIFESTACIONES CLÍNICAS DE LAS FORMAS MÁS FRECUENTES DE ESPONDILOLISTESIS
Espondilolistesis tipo II o ístmica
Este tipo representa la forma más frecuente de espondilolistesis. El prototipo de paciente es un mujeres jovenes, generalmente deportista. Su causa es la denominada espondilólisis, que hace referencia a una fractura o elongación de la pars interarticularis, que es una pequeña porción de hueso vertebral que conecta las apófisis articulares superior e inferior. La pars interarticularis tiene un escaso suministro de sangre, lo cual hace que sea muy susceptible a sufrir fracturas, que generalmente se producen por un mecanismo de fatiga y estrés por microtraumatismos de repetición. La localización más frecuente es L5-S1. Está presente en el 5% de los Europeos, en el 50% de los esquimales y en mujeres jóvenes que realizan deportes de hiperextensión como gimnasia rítmica o equitación. Clínicamente suele manifestarse con dolor en la zona lumbar, contracturas de los músculos isquiotibiales, limitación para flexionar el tronco y alteraciones en la marcha. Así mismo, puede aparecer deformidad de la columna y pérdida de la lordosis lumbar en aquellos casos con desplazamientos importantes. Los síntomas neurológicos, tales como dolor radicular o datos de compromiso medular son en general infrecuentes, presentándose en aquellos pacientes con desplazamientos muy graves o en los que existan otras patologías concomitantes como puede ser una hernia discal. La espondilólisis puede detectarse en las radiografías oblicuas con un signo radiográfico al que se suele hacer referencia como “borramiento del cuello del perrito escocés o de LaChapelle”. En función del grado de desplazamiento la clínica es variable. Así, las espondilolistesis de grado I y II normalmente cursan con dolores episódicos, mientras que en los grados III y IV suele aparecer un dolor constante y prolongado, habitualmente acompañado de deformidad en la columna y otras manifestaciones que conllevan mayor limitación, como alteraciones en la marcha o contracturas de isquiotibiales. Es importante destacar que no toda espondilólisis se acompaña de espondilolistesis, es más, la forma más frecuente de presentación de una espondilólisis por fatiga típica de los pacientes jóvenes es un dolor lumbar local sin otras manifestaciones clínicas ni radiográficas. En caso de sospecha clínica, las técnicas de imagen de elección para valorar la columna vertebral y especialmente la zona de la pars interarticularis son la radiografía simple, la TC y en ocasiones el SPECT. En caso de clínica neurológica se debe valorar el estado de las raíces nerviosas y de la médula espinal con una resonancia magnética.Espondilolistesis tipo III o degenerativa
Representa la segunda forma más frecuente de espondilolistesis. En este caso, los pacientes suelen ser mujeres de edad avanzada. La etiología de este tipo de espondilolistesis son cambios degenerativos asociados al envejecimiento en articulaciones facetarias y discos intervertebrales que ocasionan inestabilidad y propician los desplazamientos. Entre los cambios degenerativos más destacables que participan en este tipo de espondilolistesis se encuentran la degeneración discal, la disfunción de los ligamentos, la artrosis de las articulaciones facetarias y la ineficacia de los músculos en su función estabilizadora. El cuerpo vertebral se desliza anteriormente sobre la vertebra inferior como consecuencia de la sagitalización de las facetas articulares. La localización más habitual de la espondilolistesis degenerativa es L4-L5. Hay algunos datos epidemiológicos a destacar respecto a este tipo de listesis, en primer lugar, raramente aparece en personas menores de 50 años, las mujeres tienen mucho más riesgo de padecerla que los varones, con una relación 5:1 y las personas de raza negra están más afectadas que las de raza caucásica. Así mismo, en mujeres se ha encontrado que existe una relación significativa entre un índice de masa corporal en rango de sobrepeso o superior y la presencia de espondilolistesis degenerativa, no así en varones. No se ha descrito una asociación entre espondilolistesis degenerativa y exposición ocupacional a cargas repetidas de peso en la zona lumbar. La gravedad de las manifestaciones clínicas no es proporcional ni se correlaciona con el grado de desplazamiento, además, no siempre se producen manifestaciones clínicas, pues los deslizamientos vertebrales no suelen superar el 30%. El dolor lumbar vuelve a ser el síntoma fundamental en este tipo de espondilolistesis, con gran frecuencia acompañándose de clínica neurológica, fundamentalmente dolor radicular y sobre todo claudicación neurogénica, por la estenosis del canal raquídeo que se forma. En algunos casos puede llegar a aparecer un síndrome de cola de caballo de presentación insidiosa y poco manifiesta, a diferencia del que aparece de forma aguda en hernias discales. En el diagnóstico son de nuevo necesarias las pruebas de imagen radiológicas, siendo de primera elección en una sospecha de espondilolistesis degenerativa la radiografía simple, pudiendo complementar con TC . La resonancia magnética se reserva para aquellos casos con clínica neurológica.MANEJO Y TRATAMIENTO DE LAS ESPONDILOLISTESIS
Existen dos formas de tratamiento de las espondilolistesis, la conservadora y la quirúrgica. La primera consiste en el uso de ortesis, tratamiento del dolor con distintos grados de analgesia y rehabilitación. La segunda se basa en las artrodesis, es decir, en la fijación de dos porciones óseas vertebrales a través de tornillos, placas o barras con el objetivo de dotar de estabilidad a dicha zona de la columna vertebral. El tratamiento debe ser según la clínica del paciente y ser progresivo, intentando inicialmente tratamiento conservador y si fracasa optar por la cirugía La cirugía más frecuentemente empleada es la artrodesis o fijación lumbar con tornillos pediculares, se puede asociar o no a descompresión de los elementos nerviosos si existe clínica neurológica.Si quiere seguir leyendo sobre otros temas de cirugía de columna puede hacerlo en https://traumatologosalamanca.com/cirugia-de-columna/ y en https://www.doctorpescador.es/dolor-lumbar/
SI TE DUELE LA ESPALDA CONSULTENOS, CUIDAMOS TU ESPALDA CUIDAMOS DE TI.
#espondilolistesis #espondilolisis #dolorlumbar #cirugíadecolumna #spinesurgery #artrodesislumbar #herniadiscal #estenosisdecanal #traumatología #neurocirugía
BIBLIOGRAFÍA
- García-Ramos CL, Valenzuela-González J, Baeza-Álvarez VB, Rosales-Olivarez LM, Alpizar-Aguirre A, Reyes-Sánchez A. Degenerative spondylolisthesis I: general principles. Acta Ortop Mex. 2020 Sep-Oct;34(5):324-328.
- García-Ramos CL, Valenzuela-González J, Baeza-Álvarez VB, Rosales-Olivarez LM, Alpízar-Aguirre A, Reyes-Sánchez A. Lumbar degenerative spondylolisthesis II: treatment and controversies. Acta Ortop Mex. 2020 Nov-Dec;34(6):433-440.
- Maroto Rodríguez R, Chivato Vivanco F, Lorente Gómez A, Vilanova Laguna J, Copete González I, Cuervas-Mons Cantón M et al. Manual CTO de Medicina y cirugía. Traumatología y cirugía ortopédica. 11ª ed. Madrid: CTO Editorial; 2019.

ESGUINCE DE TOBILLO LA LESIÓN DEPORTIVA MÁS FRECUENTE
24 julio 2022El esguince de tobillo es la lesión traumática de los ligamentos del tobillo. Estos son el ligamento peroneo astragalino anterior (LPAA) y posterior (LPAP) y el ligamento peroneo calcáneo (LPC). Estos ligamentos pueden lesionarse de diferentes maneras, desde un simple estiramiento, a romperse parcial o completamente, variando enormemente el tratamiento y la clínica del paciente según la gravedad.
EPIDEMIOLOGÍA DEL ESGUINCE DE TOBILLO
El esguince de tobillo se considera una de las lesiones deportivas más frecuentes, suponiendo el 20% de todas ellas. También es muy común en la población general, siendo la lesión más frecuente en los servicios de Urgencias. La edad más frecuente de producción está en torno a los 15-35 años por entorsiones del tobillo en traumatismos de diferentes indoles.CLASIFICACIÓN DEL ESGUINCE DE TOBILLO
El esguince de tobillo se clasifica en 3 grados:- Grado 1 (Leve): estiramiento si rotura del ligamento. Solo se afecta el LPAA
- Grado 2 (Moderado): rotura parcial del ligamento. Se afecta el LPAA y LPC.
- Grado 3 (Severa): rotura completa del ligamento, pudiendo aparecer inestabilidad. Se afectan el LPAA, LPC y LPAP
CLINICA DEL ESGUINCE DE TOBILLO
El síntoma fundamental es el dolor, que se puede intensificar al mover el tobillo. En las torceduras graves, puede resultar imposible cargar peso sobre la pierna afectada. También puede haber una cierta hinchazón y hematoma. La hinchazón se produce poco después de la lesión, pero el hematoma puede tardar hasta 24 horas en desarrollarse completamente. La hinchazón del tobillo puede dificultar el movimiento del pie y el tobillo puede volverse inestable.CAUSAS DEL ESGUINCE DE TOBILLO
El tipo más común de torcedura de tobillo se produce cuando el pie se gira hacia dentro y estira excesivamente los ligamentos de la parte exterior del tobillo. Este tipo de torcedura es especialmente común en los deportes que requieren correr y saltar, cambios rápidos de dirección o arrancar y parar muchas veces, como el fútbol, el baloncesto y el voleibol. Caminar o correr por una superficie irregular, resbalarse del bordillo de la acera, torcerse el tobillo subiendo las escaleras o perder el equilibrio cuando se llevan tacones altos son formas de torcerse el tobillo. También existen más probabilidades de torcerse el tobillo si uno ya se lo ha torcido antes.DIAGNÓSTICO DEL ESGUINCE DE TOBILLO
El diagnóstico se realiza por la clínica y causa de producción de la lesión. Se deben realizar pruebas radiológicas como la radiografía simple, si la gravedad del esguince lo requiere, según las reglas de Ottawa. La resonancia magnética se hacen para realizar diagnósticos diferenciales o valorar criterios quirúrgicos, en tobillos inestables.DIAGNÓSTICO DIFERENCIAL
El diagnóstico diferencial debe hacerse con las siguientes patologías.- Síndrome del seno del tarso.
- Fractura del 5 metatarsiano
- Lesión condral del astrágalo.
- Tendinosis de los peroneos
- Síndrome de pinzamiento del tobillo (Tobillo del futbolista)
TRATAMIENTO DEL ESGUINCE DE TOBILLO
Tratamiento conservador
Como tratamiento inicial, descanse, ponga hielo y comprima y eleve la zona afectada. No obstante, si sus síntomas son fuertes, si, por ejemplo, tiene mucho dolor, si la parte lesionada de la pierna está extremadamente inflamada o deformada, o si no puede cargar peso sobre la misma, deberá acudir a su médico de familia o ir a urgencias. Los analgésicos y los antinflamatorios pueden ayudar para reducir el dolor y la inflamación. En la mayoría de las torceduras, el hinchazón y las molestias comenzarán a remitir al cabo de unos días. A partir de entonces deberá comenzar a mover el tobillo. Las vendas de compresión deberán quitarse al cabo de dos días porque limitan el movimiento. En su lugar puede utilizar una tobillera que no restrinja mucho el movimiento. También la fisioterapia puede ayudar en la recuperación funcional del tobillo.Tratamiento quirúrgico
El tratamiento quirúrgico se encuentra muy debatido, realizándose en casos de grado 3 y en deportistas de elite. EL 20% de los esguinces se convierten en inestables pudiendo requerir cirugía. Las técnicas de reconstrucción pasan desde reparación anatómica con sutura termino terminal o realizando plastias de refuerzo.En el siguiente link se puede ver la técnicas de reconstrucción del ligamento
https://www.arthrex.com/es/recursos/animacion/xoEL_29ozEaX0gF8o-VVxQ/internalbrace-atfl-talus-to-fibula-ligament-augmentation-repair?referringteam=foot_and_ankle
PARA SEGUIR LEYENDO MÁS SOBRE PATOLOGÍA DEL PIE Y TOBILLO PUEDE HACERLO EN https://www.doctorpescador.es/ Y EN https://traumatologosalamanca.com/
SI HAS TENIDO UNA LESION DEL TOBILLO CONSULTENOS, CUIDAMOS TU TOBILLO , CUIDAMOS DE TI.
#esguincedetobillo #lesionesdeportivas #fracturadetobillo #patologíadepie #lesióndeaquiles
BIBLIOGRAFIA
- Petersen W, Rembitzki IV, Koppenburg AG, Ellermann A, Liebau C, Brüggemann GP, Best R.Treatment of acute ankle ligament injuries: a systematic review. Arch Orthop Trauma Surg. 2013 Aug;133(8):1129-41.
- Kerkhoffs GMMJ, Rowe BH, Assendelft AJJ, Kelly K, Struis PAA, van Dijk CN (2002) Immobilisation and functional treat- ment for acute lateral ligament injuries in adults (Review) Cochrane Database Syst Rev Issue 3, Art. No. CD003762. doi:10.1002/14651858.CD003762
- Wang YT, Wu XT, Chen H. Pure closed posteromedial dislocation of the tibiotalar joint without fracture. Orthop Surg. 2013 Aug;5(3):214-8.
- Hunt KJ, Phisitkul P, Pirolo J, Amendola A. High ankle sprains and syndesmotic injuries in athletes. J Am Acad Orthop Surg. 2015; 23: 661-673.
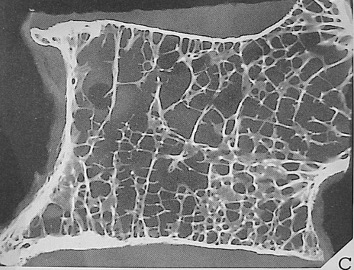
OSTEOPOROSIS: ENFERMEDAD SILENCIOSA DEL HUESO
15 junio 2022
La osteoporosis es una enfermedad caracterizada por un descenso de la densidad ósea que conlleva el debilitamiento y deterioro de la microarquitectura del tejido óseo. Esto compromete la resistencia de los huesos y predispone a las fracturas por fragilidad. Las alteraciones óseas asociadas producen un descenso en la resistencia ósea y un aumento de riesgo de fractura.
EPIDEMIOLOGÍA DE LA OSTEOPOROSIS
La osteoporosis es la enfermedad metabólica más frecuente, aunque su prevalencia no se conoce ya que en la mayoría de los casos no se diagnostica hasta que se hace sintomática por la aparición de complicaciones. Junto a las fracturas por fragilidad hay una serie de complicaciones que afectan a la calidad de vida de los pacientes y suponen un elevado impacto económico en la población de los países desarrollados. Las fracturas osteoporóticas más importantes por orden decreciente de importancia son: vértebra, cuello de fémur y antebrazo. La pérdida de densidad mineral ósea asociada a la osteoporosis es más común en las mujeres, en las que comienza de forma más temprana que en los hombres debido a la caída de estrógenos que se produce en la menopausia. En los primeros años de la menopausia, la pérdida de DMO es más rápida, pero va frenando con los años hasta igualarse y estabilizarse con la de los hombres. Sin embargo, las fracturas por fragilidad en los hombres se producen con niveles de densidad mineral ósea mayores que en las mujeres.CLASIFICACIÓN DE LA OSTEOPOROSIS
La clasificación de la osteoporosis puede hacerse según su etiología. Por un lado, la osteoporosis primaria es la más frecuente, también se la conoce como osteoporosis involutiva y se diagnostica cuando no se puede determinar la causa que produce la osteoporosis. Dentro de la osteoporosis primaria se diferencian la juvenil, la postmenopáusica, la relacionada con la edad y la idiopática. Por otro lado, la osteoporosis secundaria se diagnostica cuando la razón de la pérdida de densidad mineral ósea se atribuye a alguna causa particular como el uso de fármacos, en especial los glucocorticoides, u otras enfermedades.DIAGNÓSTICO DE LA OSTEOPOROSIS
Existen determinadas pruebas que nos permiten diagnosticar con mayor o menor fiabilidad la osteoporosis.La radiografía:
La radiografía simple no es apropiada para evaluar de forma fiable la DMO de los pacientes, debido a que requiere una valoración subjetiva y conlleva una gran variabilidad dependiendo del observador, lo que desemboca en la indicación de tratamientos en pacientes que no lo necesitan y viceversa. Sí estaría indicada la realización de una radiografía simple ante la sospecha de una fractura por fragilidad.La densitometría:
La densitometría radiológica dual o DXA puede medir las dimensiones de las vértebras en proyecciones laterales con una sensibilidad similar a la de la radiografía simple, pero con menor dosis de radiación. El diagnóstico de osteoporosis mediante DXA puede verse influido por factores diversos relacionados con la medición o posibles artefactos. Para intentar reducir el número de variables, es recomendable explorar, al menos, dos regiones del esqueleto. A menudo, la DXA se utiliza inapropiadamente para el diagnóstico de osteoporosis debido a su bajo coste económico. Pese a todo esto, la DXA central (de cadera y columna) es la prueba de referencia diagnóstica para la osteoporosis en la práctica clínica. Con la DXA se le atribuye al paciente una “T-score”:- DMO normal: T-score > -1.0
- Osteopenia: T-score entre -1.0 y -2.4
- Osteoporosis: T-score < -2.5
- Osteoporosis grave: T-score < -2.5 con una fractura por fragilidad asociada
Ultrasonometría cuantitativa o QUS:
Otra prueba diagnóstica de la osteoporosis es la ultrasonometría cuantitativa o QUS aunque, de acuerdo con la guía de práctica clínica sobre la osteoporosis, no debe ser considerada para el diagnóstico de la osteoporosis debido a su baja precisión, las medidas que ofrecen no están estandarizadas, la T-score que proporciona no se corresponde a la proporcionada por la DXA… Por último, cabe destacar la determinación de marcadores óseos para el diagnóstico de la osteoporosis, pese a que según estudios no son útiles para el diagnóstico y no se recomienda su uso sistemático para la detección de osteoporosis.TRATAMIENTO DE LA OSTEOPOROSIS
Entre las intervenciones preventivas de las fracturas de fragilidad por la osteoporosis encontramos: dieta rica en calcio, vitamina D e isoflavonas, exposición al sol, práctica de actividad física diaria, no consumo de alcohol, tabaco ni cafeína además de tratamientos farmacológicos como:- Suplementos de calcio y vitamina D
- Fármacos que evitan la resorción ósea estabilizando el hueso, como los bifosfonatos, raloxifeno, calcitonina, etc.
- Fármacos productores de hueso como la teriparatida, parathormona, etc.
- Terapias hormonales sustitutivas con estrógenos solos o combinados con progestágenos, tibolona, etc.
- Denosumab: un anticuerpo monoclonal humano que inhibe la formación, supervivencia y función de los osteoclastos disminuyendo la resorción ósea de hueso trabecular y cortical. El denosumab tiene efectos secundarios importantes como la osteonecrosis mandibular (cuyos factores de riesgo son tratamientos previos con bifosfonatos, edad avanzada, higiene bucal deficiente, procedimientos dentales invasivos, diagnóstico de cáncer con lesiones óseas, consumo de tabaco y otras comorbilidades) y la hipocalcemia, ya que el denosumab impide la liberación del calcio de los huesos a la circulación sistémica (el mayor factor de riesgo para la hipocalcemia es la insuficiencia renal).
- Otros como las estatinas, suplementos de nutrientes, etc.
EVOLUCIÓN DE LA OSTEOPOROSIS:
Una vez diagnosticada la osteoporosis, para el control de la evolución de esta se pueden realizar las mismas pruebas que para el diagnóstico de la osteoporosis. De nuevo, la densitometría radiológica dual (DXA) es la prueba de referencia para el estudio evolutivo de la osteoporosis en el esqueleto central (en la cadera y la columna). El intervalo recomendado entre los controles es, como mínimo, 2 años excepto en los pacientes con circunstancias especiales como aquellos en los que se ha realizado un trasplante de órgano sólido o en aquellos en tratamiento con glucocorticoides.FRACTURAS POR FRAGILIDAD EN LA OSTEOPOROSIS
Las fracturas por fragilidad son aquellas que se producen por impactos de baja intensidad, como caídas desde la propia altura del paciente y son la causa principal de morbimortalidad crónica de la osteoporosis. Las fracturas por fragilidad en orden decreciente de frecuencia son las siguientes: vertebrales (https://www.doctorpescador.es/fractura-vertebral/) , del cuello del fémur (https://www.doctorpescador.es/fractura-de-cadera/) y de la extremidad distal del radio (Colles)( https://www.doctorpescador.es/fractura-de-muneca-colles/ ).Factores de riesgos para las fracturas de fragilidad
Los factores de riesgo clínicos que tienen relación clara con el descenso de la densidad mineral ósea y, por tanto, están asociados al riesgo de fractura por fragilidad son: fracturas por fragilidad previas, antecedentes familiares de fractura de cadera, tener 65 años o más, IMC inferior a 20kg/m2, tratamiento con glucocorticoides, fallo ovárico sin tratar, hiperparatiroidismo, malnutrición crónica y malabsorción. Otros factores de riesgo moderado o menores asociados a las fracturas por fragilidad son: el consumo de 3 o más UBE/día, fumador actual, diabetes mellitus tipo 1, artritis reumatoide, sexo femenino y menopausia temprana.¿Cómo valorar el riesgos de presentar una fractura por osteoporosis?
En la valoración del riesgo de fractura por fragilidad, la prueba de referencia es la medición de la DMO mediante la DXA en la columna lumbar y fémur proximal, es decir, en esqueleto central. Para la estimación del riesgo de fractura a 10 años se utiliza el modelo FRAX, una herramienta que funciona en hombres y mujeres de entre 40-90 años y que, mediante un programa informático permite calcular la probabilidad de fractura por fragilidad a 10 años y específicamente en la cadera. Para el cálculo del riesgo se tienen en cuenta los siguientes factores: la edad, el sexo, el IMC, la presencia de fracturas previas, fractura de cadera de los padres, consumo actual de tabaco, tratamiento con glucocorticoides, presencia de artritis reumatoide, osteoporosis secundaria, consumo de más de 3 UBE/día y la DMO del cuello del fémur. En el caso del cálculo de riesgo de fractura vertebral por fragilidad se utiliza el algoritmo ECOSAP. Por otra parte, los factores de riesgo que se asocian frecuentemente a caídas también deben considerarse en las personas mayores pese a que no se relacionan directamente con la pérdida de DMO: edad mayor de 80 años, antecedentes de caída en el último año, deterioro cognitivo y funcional y/o sensorial, consumo de fármacos como antidepresivos, benzodiacepinas, miedo a caer, incontinencia urinaria, etc.Fractura vertebral por osteoporosis
Las fracturas vertebrales por fragilidad son muy prevalentes actualmente y general una gran pérdida de calidad de vida en nuestros mayores. El tramo vertebral más afectado está entre D4-L3. La exploración fundamental para el diagnóstico de estas es la radiografía simple lateral de la columna lumbar y dorsal. Se define fractura vertebral como la pérdida de al menos un 20% de la altura vertebral global o en su porción anterior, media y posterior con respecto a la vértebra adyacente. Su confirmación se hace mediante resonancia magnética. Signos radiológicos de las fracturas vertebrales Las fracturas vertebrales por fragilidad se acompañan de una serie de signos radiológicos sugestivos como la localización dorsolumbar, la conservación de los espacios discales, el hundimiento de las plataformas, el respeto de los pedículos vertebrales y otros signos radiológicos de hipertransparencia (reforzamiento de los platillos vertebrales y, en algunos casos, aspecto de vértebra vacía). Las fracturas osteoporóticas vertebrales son estables y no producen compresión nerviosa ni síntomas neurológicos. Clínica de las fracturas vertebrales Dos de cada tres casos de fractura vertebral osteoporótica son asintomáticos. En aquellos casos en los que se acompañan de clínica, esta es: dolor agudo incapacitante en la zona dorsolumbar que se suele presentar tras flexiones súbitas de la espalda, levantamiento de peso o incluso sin ningún sobreesfuerzo previo. En estos casos la movilidad queda reducida y no son capaces de mantenerse sentados. Es característico que el dolor aumente con maniobras de Valsalva. Tratamiento de las fracturas vertebrales El tratamiento conservador de las fracturas por fragilidad vertebrales incluye el reposo absoluto en cama hasta 3 semanas y tratamiento con analgésicos potentes. El dolor suele remitir en ese tiempo de forma parcial o total, siendo capaces de retomar su actividad habitual en torno a las 6 semanas. En otras ocasiones el paciente refiere un dolor sordo constante que empeora al realizar maniobras mecánicas. Junto a la analgesia, otra posibilidad de tratamiento conservador de las fracturas vertebrales es el uso de una faja compresiva durante 3 meses, aunque tiene sus desventajas como el hecho de que no es bien tolerada en pacientes mayores y requiere una monitorización radiológica para la detección precoz del desplazamiento vertebral que se produce a consecuencia de su uso prolongado. En cuanto a las posibilidades quirúrgicas, la cirugía mínimamente invasiva es una opción para el tratamiento de las fracturas vertebrales por osteoporosis. La característica común de estas intervenciones es su acceso percutáneo mediante la canulación del pedículo controlada por imágenes intraoperatorias. Por último, las técnicas de cementoplastia varían desde la inyección simple de cemento (vertebroplastia) al uso de balones de reducción (cifoplastia) a la inserción de un implante como un stent. Este tipo de intervenciones tiene la ventaja de que pueden utilizarse en pacientes frágiles y en varios niveles de la columna de forma simultánea además de que presentan unos resultados analgésicos postoperatorios casi inmediatos, una vez que el cemento queda polimerizado. Sin embargo, estas intervenciones tienen una serie de contraindicaciones, como los casos de colapso total del cuerpo vertebral, cuando existe déficit neurológico o afectación de la pared posterior, etc. El el 10-80% de los casos presenta complicaciones relacionados con la fuga del cemento lo que puede producir diferentes consecuencias según la localización del trombo, siendo el más común un tromboembolismo pulmonar.CONCLUSIÓN
La prevención de la osteoporosis es una gran preocupación en el ámbito de la salud actualmente. La disminución de la DMO se produce tanto en mujeres como en hombres a lo largo de la vida desencadenada por déficits hormonales, de calcio y cambios en la formación de los huesos. Hoy en día, el diagnóstico de la osteoporosis puede hacerse antes de que se produzcan las fracturas por fragilidad, lo que hace posible el tratamiento y la prevención de estas. Cabe destacar la importancia de la individualización del tratamiento entre pacientes, debido a que se conoce la existencia de diversos tipos de osteoporosis además del hecho de que el comportamiento de una osteoporosis de comienzo reciente no es el mismo que el de una de varios años de evolución en la que lo más probable es que se acompañe de fracturas por fragilidad. Por último, el desarrollo de nuevos fármacos que impiden la resorción ósea y facilitan la formación del hueso como el Denosumab abre las puertas hacia un futuro prometedor en el tratamiento de la osteoporosis, impidiendo la evolución de la enfermedad de un elevado número de pacientes.SI TIENES OSTEOPOROSIS O FRACTURAS POR FRAGILIDAD CONSULTENOS, CUIDAMOS SUS HUESOS, CUIDAMOS DE TI.
Si quiere leer sobre artículos relacionados puede hacerlo en https://traumatologosalamanca.com/traumatologia-cirugia-ortopedica/ #osteoporosis #fracturas #colles #fracturavertebral #cifoplastia #nopuedocaminar #fracturadecadera.Bibliografía:
- Lane JM, Russell L, Khan SN. Osteoporosis. Clin Orthop Relat Res [Internet]. 2000;372(372):139–50. Disponible en: https://pubmed.ncbi.nlm.nih.gov/10738423/
- Denosumab: riesgo de osteonecrosis mandibular e hipocalcemia - Agencia Española de Medicamentos y Productos Sanitarios [Internet]. Agencia Española de Medicamentos y Productos Sanitarios. Disponible en: https://www.aemps.gob.es/informa/notasinformativas/medicamentosusohumano-3/seguridad-1/2014/ni-muh_fv_13-2014-denosumab/
- Kanis JA, on behalf of the Scientific Advisory Board of the European Society for Clinical and Economic Aspects of Osteoporosis (ESCEO) and the Committees of Scientific Advisors and National Societies of the International Osteoporosis Foundation (IOF), Cooper C, Rizzoli R, Reginster J-Y. European guidance for the diagnosis and management of osteoporosis in postmenopausal women. Osteoporos Int [Internet]. 2019;30(1):3–44. Disponible en: http://dx.doi.org/10.1007/s00198-018-4704-5
- Friedman SM, Mendelson DA. Fragility fractures. Clin Geriatr Med [Internet]. 2014;30(2): xiii–xiv. Disponible en: https://www.geriatric.theclinics.com/article/S0749-0690(14)00020-2/fulltext
- Hermoso de Mendoza MT. Clasificación de la osteoporosis: Factores de riesgo. Clínica y diagnóstico diferencial. An Sist Sanit Navar [Internet]. 2003; 26:29–52. Disponible en: https://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S1137-66272003000600004
- Prost S, Pesenti S, Fuentes S, Tropiano P, Blondel B. Treatment of osteoporotic vertebral fractures. Orthop Traumatol Surg Res [Internet]. 2021 [;107(1S):102779. Disponible en: https://pubmed.ncbi.nlm.nih.gov/33321233/
- De G, Clínica P, El EN. Guía de Práctica Clínica sobre Osteoporosis y Prevención de Fracturas por Fragilidad [Internet]. Seiomm.org. [cited 2022 Apr 4]. Available from: https://seiomm.org/wp-content/uploads/2020/04/Gui%CC%81as-de-pra%CC%81ctica-cli%CC%81nica-en-el-SNS
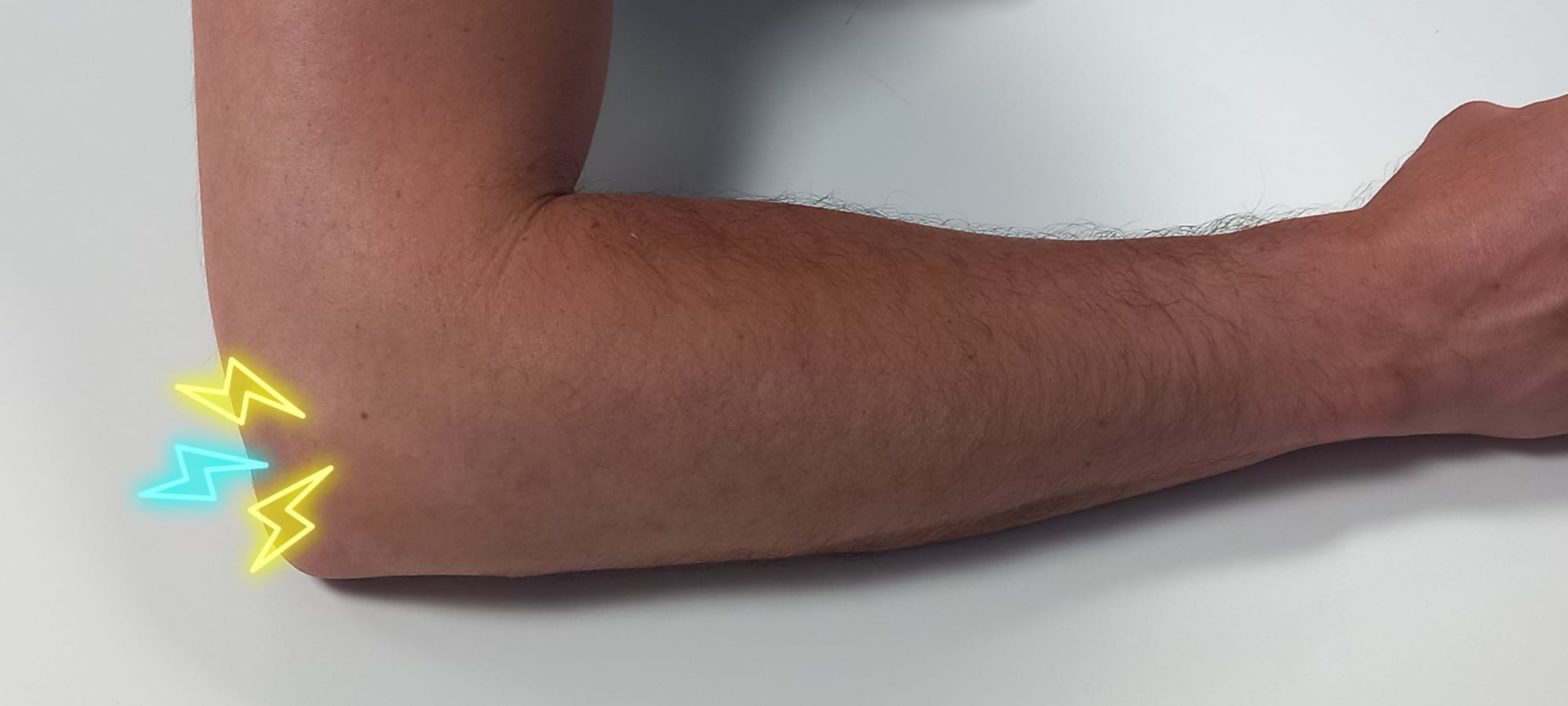
EPICONDILITIS O “CODO DE TENISTA”
11 mayo 2022La epicondilitis es la inflamación de la inserción proximal de los músculos epicondíleos del codo que puede aparecer como consecuencia de un traumatismo, o debido a la sobrecarga por movimientos repetitivos, en ocasiones relacionados con ciertos oficios o deportes (como el tenis, por ello se le conoce como “codo de tenista”).
Los pacientes presentan dolor selectivo a la palpación en el epicóndilo, que aumenta al extender los dedos contra resistencia. A veces este dolor puede irradiarse por la cara externa del brazo y antebrazo.
La prevalencia de esta patología es del 1-3% de la población adulta al año, con una mayor incidencia entre los 35 y 50 años, sobre todo en el brazo dominante.
CAUSAS DE LA EPICONDILITIS
El mecanismo etiopatogénico de la tendinopatía epicondílea no está completamente claro, y en muchos casos no se puede identificar la causa. A pesar de conocerse como “codo de tenista” los jugadores de tenis representan únicamente un pequeño porcentaje de los pacientes, ya que la mayoría no realizan actividades profesionales con movimientos repetitivos o soporte de pesos. Por tanto, suelen aparecer en pacientes adultos, tras un traumatismo o como consecuencia de la artritis reumatoide. Sin embargo, un porcentaje de los pacientes sí están sometidos a movimientos repetitivos de extensión de la muñeca o de supinación de la mano a partir de la posición de pronación, que realizan en ciertas profesiones manuales o en deportes muy variados que requieren sobreuso. La causa más frecuente de esta lesión son las contracciones excéntricas de la musculatura extensora del antebrazo.FACTORES DE RIESGO DE EPICONDILITIS
Además, existen ciertos factores predisponentes (genéticos, poco flujo sanguíneo); intrínsecos (edad, sexo, patologías osteoarticulares, enfermedades sistémicas que afectan a la microcirculación o al metabolismo del colágeno, estado nutricional) y extrínsecos (fuerte actividad, condiciones ambientales, errores en el entrenamiento, inmovilización) que pueden contribuir al desarrollo de la epicondilitis.¿EL “CODO DE TENISTA” ES UNA EPICONDILITIS FRECUENTE?
Los jugadores de tenis representan solamente el 5-10% de los pacientes con epicondilitis, sin embargo, está demostrado que los deportes de raqueta aumentan el riesgo de desarrollar esta tendinopatía. Las contracciones excéntricas del extensor radial corto durante el golpe de revés (flexión dorsal forzada con la mano en supinación) ocasionan un trauma repetitivo que causa la microrrotura en el tendón de este músculo, además, en el electromiograma se ha observado una mayor actividad en los músculos extensores de muñeca, lo que predispone a la lesión.TRATAMIENTO DE LA EPICONDILITIS
TRATAMIENTO CONSERVADOR
Entre un 70 y 95% de los pacientes mejoran en un periodo de meses a dos años con tratamiento conservador e incluso sin realizar ninguna terapia. Es fundamental tratar la causa y si es posible modificar las conductas y ejercicios que lo provocan. Existe multitud de tratamientos conservadores como por ejemplo:- La fisioterapia con masaje, TENS, onda corta... pueden mejorar la sintomatología.
- Ondas de choque: intentan romper las inserciones y calcificaciones. Se realizan entre 3-5 sesiones. Suelen ser un tratamiento eficaz.
- Ortesis (cinchas y férulas): las cinchas de epicondilitis ejercen su función por un mecanismo mecánico reduciendo la carga y las fuerzas que actúan en el epicóndilo, y además ayudan en la propiocepción. Las más utilizadas son las que rodean la inserción del extensor radial corto y del extensor común de los dedos por medio de una banda de compresión aplicada unos centímetros distales a la inserción de estos tendones para reducir la fuerza de tracción que se transmite a través de la unión musculo-tendinosa.
- Infiltraciones con corticoides: se suele utilizar dexametasona o betametasona , que pueden ir asociadas o no a anestésicos locales. Se pueden inyectar en la zona periepicondilar o intramuscular.
- Toxina botulínica: no hay consenso respecto a su uso, eficacia, dosis, o zona de administración.
- Otros tratamientos que aún no tienen evidencia clara son: la proloterapia (inyección de irritantes osmóticos como la dextrosa), el plasma rico en plaquetas e inyección de sangre autóloga, Tenex (aplicación de ultrasonidos), ácido hialurónico, embolización selectiva de vasos, tenotomía percutánea, etc.
TRATAMIENTO QUIRÚRGICO
Se estima que aproximadamente el 5%-10% de los pacientes son subsidiarios de tratamiento quirúrgico de la epicondilitis, ante la persistencia de dolor e impotencia funcional a pesar de haber realizado un tratamiento conservador adecuado durante un tiempo mayor a 6 meses. El desarrollo de la técnica artroscópica y la tendencia actual a la cirugía mínimamente invasiva han supuesto nuevas perspectivas en el abordaje quirúrgico de la epicondilitis, posibilitado distintas técnicas, tanto por vía percutánea como artroscópica o cirugía abierta. La elección de un método u otro está condicionada por la experiencia del cirujano con la técnica, los medios disponibles o las preferencias del paciente. En cuanto a la cirugía a cielo abierto, la técnica quirúrgica por excelencia es la resección del tejido patológico a nivel de la entesis del extensor radial corto. Este tratamiento quirúrgico mediante la liberación tendinosa es altamente efectivo, con resultados superiores al 80% de los casos y baja tasa de complicaciones. El TRATAMIENTO ARTROSCÓPICO En el tratamiento por artroscopia de la epicondilitis se realiza el mismo procedimiento que en la cirugía abierta, pero permitiendo una cirugía mínimamente invasiva, menos agresiva y con capacidad de tratar patologías asociadas intraarticulares. Los resultados del tratamiento artroscópico son satisfactorios en un alto porcentaje de casos, con la ventaja de que el paciente presenta un menor dolor postoperatorio, por lo que puede iniciar la rehabilitación de forma precoz, y el retorno a las actividades laborales y deportivas se realiza en un periodo de tiempo más corto. A pesar de estas ventajas de la técnica artroscópica, hay que tener en cuenta que es válida en manos expertas y en centros donde el volumen de casos sea importante, ya que requiere de una curva de aprendizaje importante. En general el tratamiento quirúrgico suele dar buenos resultados, sin embargo, no existen evidencias claras a favor del empleo de una técnica quirúrgica determinada, ya sea cirugía abierta, percutánea o artroscópica. Puede seguir leyendo en https://www.doctorpescador.es/ SI TE DUELE EL CODO CONSULTENOS, CUIDAMOS TU CODO CUIDAMOS DE TI. Si quiere leer sobre otras lesiones deportivas puede hacerlo en https://traumatologosalamanca.com/medicina-del-deporte/ #cododetenista #epicondilitis #tendinitis #Salamanca #Zamora #medueleelcodo #artroscopia #codoBIBLIOGRAFÍA
-
- Shiri R, Viikari-Juntura E, Varonen H, Helioövaara M. Prevalence and determinants of lateral and medial epicondylitis: a population study. Am J Epidemiol. 2006;164:1065-74
- Mens JM, Stoeckart R, Snijders CJ, Verhaar JA, Stam HJ. Tennis elbow, natural course and relationship with physical activities: an inquiry among physicians. J Sports Med Phys Fitness. 1999;39:244-8
- Cañellas A, Terré RA, Bernet L, Badía N, Parrilla G. Epicondilitis crónica (parte II): tratamiento quirúrgico, valoración de resultados y revisión bibliográfica. Avances 1993; 23/2: 98-106
- Bacle G, Marteau E, Laulan J. Cirugía de las lesiones tendinosas y ligamentarias del codo. EMC - Técnicas Quirúrgicas - Ortopedia y Traumatología. 2015; 7(1): 1-18
- Carratalá V, Lucas FJ, Miranda I, Ortego JI, Sánchez-Alepud E. Tratamiento artroscópico versus tratamiento mediante cirugía abierta de la epicondilitis lateral. Estudio de cohortes prospectivo. Rev esp artrosc cir articul 2016; 23(2): 96–102
- Stiefel EC, Field LD. Arthroscopic lateral epicondylitis release using the bayonet technique. Arthrosc Tech 2014;3:e135–9.
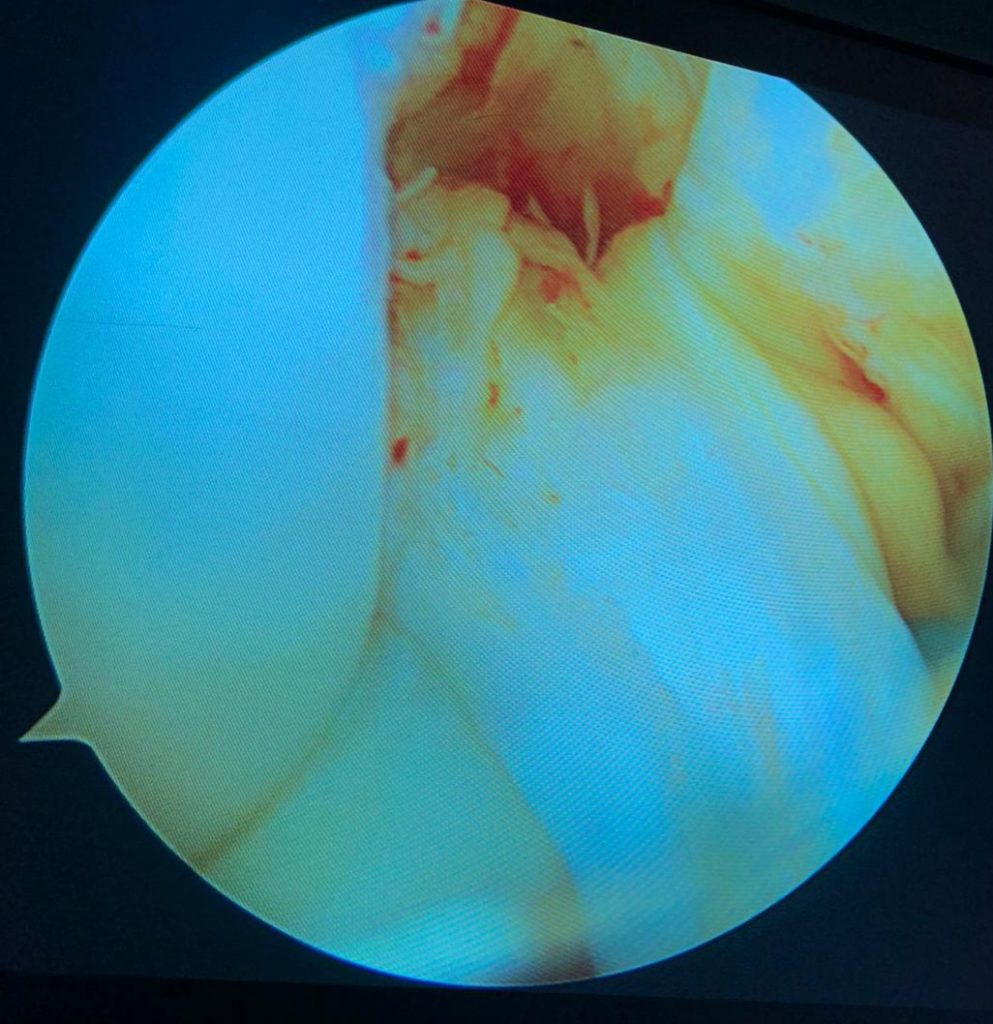
ROTURA DEL LIGAMENTO CRUZADO ANTERIOR, UNA LESION DEPORTIVA DE LA RODILLA MUY FRECUENTE
16 abril 2022Las lesiones deportivas de la rodilla son muy frecuentes y la rotura del ligamento cruzado anterior (LCA) es una de ellas. Suele producirse en múltiples deporte del contacto como el futbol, baloncesto, balonmano, esquí… al dejar fijo el pie y girar bruscamente la rodilla, produciendo una desinserción de la zona femoral. Es un lesión inherentemente quirúrgica en pacientes jóvenes deportistas con inestabilidad.
ANATOMIA DEL LIGAMENTO CRUZADO ANTERIOR (LCA)
El ligamento cruzado anterior es un ligamento de fibras de colágeno que se sitúa en la región intercondílea de la rodilla y une el fémur con la tibia, dando estabilidad a la rodilla. El LCA tiene su inserción en una carilla de la parte anterior del área intercondílea de la tibia, y asciende en sentido posterior, de delante hacia atrás, para insertarse en una carilla de la porción posterior de la parte lateral de la fosa intercondílea del fémur, es decir, conecta la parte posterior-lateral del fémur con la parte antero-medial de la tibia, pasando por detrás de la rótula. Este ligamento cruza lateral al ligamento cruzado posterior (LCP) a su paso a través de la región intercondílea. La fusión fundamental del ligamento cruzado anterior es evitar el desplazamiento anterior de la tibia sobre el fémur y dar estabilidad a la rodilla cuando se produce la rotación de la misma. Limita la rotación tibial y la angulación interna y externa de la rodilla cuando se encuentra estirada.EPIDEMIOLOGÍA DE LA ROTURA DEL LIGAMENTO CRUZADO ANTERIOR
De los cuatro ligamentos más importantes de la rodilla, el ligamento cruzado anterior es el que más frecuentemente se lesiona. Es una lesión muy común en la segunda y tercera década de la vida, predominando en el sexo masculino. Cualquier cambio brusco en la dirección de la rodilla, al desacelerar, puede provocar una lesión de este ligamento. Suele lesionarse en traumatismos con hiperextensión o valgo y rotación de la rodilla. Es frecuente que se produzca durante la realización de actividades deportivas, sobre todo en aquellos deportes que implican detenerse o cambiar de dirección de forma repentina y brusca, saltar y aterrizar.CÓMO ES LA CICATRIZACIÓN LIGAMENTARIA CRUZADO ANTERIOR
Es importante conocer el proceso de cicatrización de los ligamentos para el tratamiento y rehabilitación de las lesiones. La capacidad de cicatrización de los ligamentos depende de la irrigación, la del tejido, el estrés generado durante la lesión y la cronología de este estrés. Es un proceso similar al de otros tejidos:- Reacción inflamatoria inicial: se caracteriza por vasodilatación, aumento de la permeabilidad capilar y migración de células en respuesta a sustancias como la serotonina, histamina y prostaglandinas.
- Reparación y regeneración: comienza la cicatrización del ligamento. Al principio el colágeno es tipo III, pero posteriormente es colágeno tipo I. Entre las semanas 3 y 6 disminuye el número y tamaño de los fibroblastos.
- Remodelación y maduración: entre las semanas 14 y 40.
CÚAL ES LA CLÍNICA Y LA SINTOMATOLOGÍA DE LA ROTURA DEL LIGAMENTO CRUZADO ANTERIOR
El paciente suele percibir un chasquido (“pop”) en el interior de la rodilla tras un giro brusco o un traumatismo. Desarrollan un hemartros en el periodo de tiempo de 1-2 horas, se le genera un derrame importante que le limita la flexión y extensión de la rodilla. Sensación de inestabilidad de la rodilla, fallos de rodilla con movimientos básicos o al hacer deporte. Inflamación y dolor. En muchas ocasiones en las que se produce un desgarro completo el paciente puede también no sentir dolor. Dificultad para apoyar la extremidad afectada. Puede existir limitación de los movimientos normales de la rodilla. Cuando se produce la fractura de este ligamento es frecuente que se encuentre asociada con la fractura del margen tibial lateral (Fractura de Segond), la cual es indicativa de lesión del ligamento cruzado anterior y del menisco.CÓMO DIAGNOSTICAMOS LA ROTURA DEL LIGAMENTO CRUZADO ANTERIOR
SÍNTOMAS DEL AL ROTURA DE LIGAMENTO CRUZADO ANTERIOR
El examen de la rodilla puede ser muy difícil debido a la tumefacción, dolor y espasmo muscular. Antes de examinar la rodilla lesionada hay que evaluar la normal para observar el grado de movimiento. Se debe investigar deformidad evidente, como aparecen en la luxación de la rodilla o de la rótula. La lesión aguda del LCA provoca, como ya se ha mencionado, hemartrosis (derrame) aguda dentro de las primeras horas de la lesión y, aunque no es patognomónico, es altamente sugestiva de ruptura del LCA. En caso de ruptura significativa de la cápsula sinovial, puede haber extravasación de sangre hacia las partes blandas circundantes y en ocasiones no hay derrame. Un derrame intraarticular provoca la tumefacción simétrica de toda la rodilla, que suele ser visible en la etapa aguda. No debe ser aspirado a menos que un gran derrame dificulte el examen o cause muchas molestias. Además de la tumefacción, el espasmo de los músculos isquiosurales provoca cojera. Es importante recordar que una lesión aguda del LCA podría no impedir la estabilidad funcional durante la bipedestación y la marcha, y no se debe tomar en consideración esta capacidad para descartar una lesión del LCA.EXPLORACIÓN DE LA ROTURA DEL LIGAMENTO CRUZADO ANTERIOR
Existen una serie de técnicas y signos que pueden ayudar al diagnóstico y que se basan en pruebas de estabilidad:- Maniobra de Lachman: es la prueba más sensible y específica. El paciente debe estar en decúbito supino sobre la mesa de exploración, con la rodilla flexionada aproximadamente 30 grados, en rotación externa. Con una mano se sujeta el extremo distal del muslo y con la otra el extremo superior de la tibia. Con el pulgar de la mano colocado sobre la tuberosidad tibial se deben mover de forma simultánea la tibia hacia adelante y el muslo hacia atrás, observando el grado de desplazamiento anterior de la tibia. Se debe comparar el grado de desplazamiento anterior con el de la rodilla contraria. Un excesivo desplazamiento anterior indica una rotura del ligamento cruzado anterior.
- Test del cajón anterior: La rodilla en 90º, se comparan las características de las dos rodillas en reposo, determinándose el grado de excursión así como la presencia de un punto final. (Menos sensible). Frecuentemente una caída hacia atrás de la tibia en posición de reposo, indica laxitud del ligamento cruzado posterior, apareciendo una concavidad debajo de la rótula.
- Test de Lille o Maniobra de la Palanca: Al igual que el anterior método, confirma una rotura de LCA. Esta maniobra consiste en presionar el cuádriceps del paciente, haciendo palanca sobre el puño del explorador bajo el gemelo. Para que la pierna se hiperextienda y el talón se levante de la camilla el cruzado debe estar intacto. Este test puede resultar ser un falso negativo en ocasiones.
- Fenómeno de resalte (pivot shift): en caso de tratarse de una inestabilidad crónica puede detectarse este fenómeno por subluxación tibial rotatoria al flexionar y extender la rodilla, forzando el valgo. Sospechar de lesión del LCA si existe bostezo al forzar el valgo o el varo, con la rodilla en extensión completa.
EVALUACIÓN RADIOLÓGICA DE LA ROTURA DEL LIGAMENTO CRUZADO ANTERIOR
- Radiografías: no muestran la lesión en los ligamentos, pero sirven para descartar fracturas óseas. En una placa AP podría verse la ya comentada fractura de Segond, en caso de existir.
- Artrografía: es una técnica que se utilizaba en el pasado para confirmar el estado del LCA y obtener información acerca del estado de los meniscos. Sin embargo, esta técnica ha sido reemplazada por la RMN.
- Ecografía: visualización de estructuras internas a través del uso de ondas de ultrasonido.
- RESONANCIA MAGNÉTICA NUCLEAR (RMN): es la prueba diagnóstica de confirmación de la lesión del ligamento. La mejor forma de evaluar el LCA es a través de proyecciones sagitales. Esta prueba es considerada la prueba diagnóstica de elección.La RMN ayuda al diagnóstico de la lesión de los ligamentos de la rodilla, pero es también muy importante para evaluar los meniscos de un paciente candidato a tratamiento conservador de una lesión del LCA.Las ventajas de la RMN sobre la artrografía, son su carácter no invasivo, la ausencia de radiación ionizante, la capacidad para obtener imágenes en varios planos, la independencia del operador y la rapidez para la obtención de imágenes. Las únicas contraindicaciones serían la presencia de un marcapasos cardiaco o clips para aneurisma intracraneal. La claustrofobia es una contraindicación relativa.
CÚAL ES EL TRATAMIENTO DE LA ROTURA DEL LIGAMENTO CRUZADO ANTERIOR
El objetivo del tratamiento de la rotura del ligamento cruzado es evitar la inestabilidad articular. Esta inestabilidad de la rodilla mantenida en el tiempo, además de condicionar la actividad física, produce artrosis precoz de rodilla. Se deben recuperar las funciones del LCA y proteger los meniscos y el cartílago. Existe para ello tratamiento conservador y tratamiento quirúrgico, en función de las características y expectativas del paciente.TRATAMIENTO CONSERVADOR
El tratamiento conservador se utiliza en el tratamiento inicial con el objetivo de recuperar la movilidad y potenciar la musculatura, en un intento de compensar la lesión ligamentosa, que no cicatriza. Tras la lesión se recomienda realizar lo siguiente:- Reposo. El descanso general es necesario para la recuperación y limita el peso que debe soportar la rodilla.
- Hielo. Cada dos horas, durante 20 minutos cada vez.
- Compresión.
- Elevación.
- Fortalecimiento muscular del cuádriceps y los isquiotibiales.
- Ejercicios de propiocepción
TRATAMIENTO QUIRÚRGICO
Se indicará el tratamiento no conservador en una serie de pacientes a los que habrá que identificar. Estos son aquellos que tienen más probabilidad de presentar problemas en el futuro. El cirujano debe considerar la edad, la actividad deportiva y las futuras expectativas del paciente. Hay ciertos factores de alto riesgo de resultados malos con un tratamiento conservador. Por ejemplo, un individuo joven, con un alto nivel de actividad, que no quiere modificar su estilo de vida impondrá altas exigencias funcionales a la rodilla, por eso son estos tipos de pacientes en los que estará indicada la cirugía.TRATAMIENTO QUIRÚRGICO PRECOZ O REPARACIÓN PRIMARIA
La cirugía para las lesiones del ligamento cruzado anterior (LCA) implica la reconstrucción o reparación del mismo.- La cirugía de reconstrucción del LCA utiliza un injerto para sustituir el ligamento. Los injertos más comunes son los autoinjertos, que proceden del propio paciente (tendones isquiotibiales o rotuliano). Otra opción es realizar un aloinjerto a partir de un donante fallecido.
- Normalmente la cirugía de reparación se utiliza solo en el caso de fractura por avulsión (el ligamento arranca un pequeño trozo de hueso al que está adherido).
ARTROSCOPIA PARA EL TRATAMIENTO DE LA ROTURA DEL LIGAMENTO CRUZADO ANTERIOR
La técnica es mínimamente invasiva y utiliza tejidos prescindibles. Pueden utilizarse tendones del semitendinoso y recto interno del muslo. También se puede recurrir al tendón rotuliano o a los tendones isquiosurales. El uso de los tendones isquiosurales evita la ruptura del mecanismo extensor junto con las posibles complicaciones asociadas a esta. Estos tendones son fáciles de obtener, son un tejido biomecánicamente sólido y su uso está asociado a menor morbilidad. Como ya hemos dicho, las ventajas que ofrece el procedimiento a través de artroscopia son incisiones más pequeñas, visualización de la patología intraarticular asociada, menor dolor posoperatorio y una recuperación y rehabilitación más rápidas.- Lo primero de todo, con el paciente en decúbito dorsal y bajo anestesia general o epidural, se procede a obtener por abordaje antero-medial el tejido del injerto que se haya seleccionado.
- Durante la reconstrucción artroscópica del LCA, se realizan varias incisiones pequeñas, dos o tres, alrededor de la rodilla.
- A continuación, se introduce un artroscopio dentro de una de las otras incisiones. Una cámara en el extremo del artroscopio transmite imágenes desde el interior de la rodilla a una pantalla de televisión situada en el quirófano. A través de los otros dos orificios se introducen un instrumento de irrigación y uno de recorte.
- Al realizar la técnica lo primero que se hace es confirmar el diagnóstico, pues resulta un método muy preciso para la ruptura del LCA. También podrían observarse las lesiones meniscales que existieran, y, en este caso, repararlas.
- Se perforan con guías y brocas unos pequeños agujeros en el fémur y en la tibia donde estos huesos se acercan unos a otros en la articulación de la rodilla. Los agujeros forman túneles a través de los cuales se fijará el injerto. Es de gran importancia posicionar correctamente los túneles por donde discurre la plastia para reproducir al máximo la anatomía normal del LCA y, por tanto, su función.
- Se tira del injerto a través de los túneles que se perforaron en los huesos de la parte superior e inferior.
- Se asegura el injerto con tornillos o grapas y se cierran las incisiones con puntos de sutura.
RECUPERACIÓN DE LA CIRUGÍA DE LA ROTURA DEL LIGAMENTO CRUZADO ANTERIOR
Tras la intervención, el movimiento se inicia el primer día de postoperatorio, con un aparato de movimiento continuo pasivo (AMC) de 0º a 90º. Se aumentará la amplitud del movimiento en función de la tolerancia del paciente, se retira el drenaje. Comienza la deambulación con muletas con carga de peso progresiva. Este día, además, se inician la flexión activa hasta 90º y la extensión pasiva asistida hasta 0º. Los pacientes suelen ser dados de alta el día siguiente de la intervención, con una ortesis con de control del flexo extensión. A las 2 semanas después de la cirugía se realiza la primera visita a la consulta y en las semanas siguientes se incorporan ejercicios de cadena cerrada. A las 6 semanas se modifica la ortesis retirándola generalmente. Se realizarán también en este momento ejercicios de resistencia con contracción del cuádriceps entre 90º y 40º y de los músculos isquiosurales de 0º a 90º. En el 5º mes se inicia la carrera en línea recta y salto a la cuerda, y, en el 6º mes, suele darse el alta permitiendo la actividad deportiva. Si quiere leer más sobre otras lesiones deportivas de la rodilla puede hacerlo en el siguiente link https://www.doctorpescador.es/rotura-de-menisco-sutura-meniscal-y-meniscectomia/ y https://traumatologosalamanca.com/medicina-del-deporte/las-4-claves-de-la-rotura-de-menisco/SI TIENES ALGUNA LESION DE RODILLA CONSÚLTENOS , CUIDAMOS TU RODILLA, CUIDAMOS DE TI.
#nopuedocaminar #rodilla #roturadeligamentocruzadoanterior #Zamora #Salamanca #artroscopiaderodilla #medicinadeportiva #lesionesdeportiva #traumatologo #traumatología #roturameniscal
Síndrome de espalda fallida: “la cirugía de espalda esta bien pero me sigue doliendo”.
16 marzo 2022Según la Asociación Internacional para el Estudio del Dolor, el síndrome espalda fallida o en inglés “Fail Back Surgery Syndrom (FBSS)” se define como dolor lumbar de origen desconocido que puede persistir después de una operación o aparecer en el nivel operado después de la intervención quirúrgica.1
FBSS afecta entre 10% hasta 40% de pacientes después de una operación de la espalda pero es muy difícil estimar la incidencia de síndrome de espalda fallida por la definición inexacta y la etiología heterogénea.2-5
Causas del Síndrome de espalda fallida
La etiología del síndrome es muy compleja y no bien conocida. Los factores predisponentes se pueden clasificar en preoperatorios, postoperatorios o factores durante la operación.1- Factores preoperatorios son por ejemplo ansiedad, depresión, obesidad y hallazgos físicos como estenosis o fibrosis. Los factores psicológicos tienen la influencia más grande.6,7 Además, el riesgo de padecer síndrome de espalda fallida aumenta con la decisión de intervenirse con un cirujano inadecuado para ejecutar la operación.8
- Factores durante la operación incluyen operar el nivel vertebral incorrecto o solo operar un nivel vertebral aunque el dolor tiene su origen en varios.8 El Síndrome de espalda fallida puede ser causado por complicaciones durante la operación, aumentando síntomas precedentes o causar nuevas causas como la inestabilidad espinal o fibrosis epidural.9 La generación de estenosis foraminal es considerada como la anomalía estructural más común que causa síndrome de espalda fallida en pacientes intervenidos.10
Diagnóstico de síndrome de espalda fallida
El diagnóstico empieza con una anamnesis y un examen físico preciso, donde los primeros pasos son determinar la región y la gravedad del dolor. Se pone el dolor en relación temporal con la operación que puede dilucidar el diagnóstico diferencial.8 Un ejemplo es el dolor radicular preoperatorio que persiste después de la operación y puede indicar un nivel incorrecto o cirugía incompleta. Otro ejemplo es dolor radicular de nuevo comienzo inmediatamente después de la operación como posible signo de un tornillo mal colocado. Por limitaciones en el examen físico es necesario hacer diagnóstico con imagen. 1La radiografía simple
Como primera prueba diagnóstica, se hace una radiografía simple para evaluar el dolor lumbar crónico postoperatorio, con el que se puede ver deformidades espinales, cambios de la lordosis y balance sagital.11 Las limitaciones de la radiografía son el fallo de representar las tres dimensiones o el tejido blando que lo hace inadecuado para conocer estenosis espinal, deformidades discales o un pinzamiento de la raíz nerviosa.8El TAC y la RMN
La imagen avanzada se realiza con RMN con o sin contraste, que hace posible una diferenciación entre una herniación discal o una fibrosis postoperatoria como posible causa del dolor lumbar y, en general, es la modalidad preferida para visualizar tejidos blandos.12 Suplementariamente, el TAC puede ayudar con cambios óseos como por ejemplo en las facetas o de las dimensiones óseas del canal., así como valorar la disposición de los tronillos pediculares.13 Una parte de los procedimientos del diagnóstico forman los bloqueos nerviosos , que pueden ser usados para el diagnóstico y para el tratamiento 14 . Con la adición de esteroides en la inyección, el bloqueo puede ser diagnóstico y terapéutico.15Tratamiento del síndrome de espalda fallida
El tratamiento del síndrome de espalda fallida puede ser conservador o quirúrgico, siempre debe empezar por el conservador y si no hay indicación para una cirugía de emergencia.16Tratamiento conservador
Por un lado, el tratamiento conservador consiste en fármacos incluyendo antiinflamatorios no esteroides (AINEs), opiáceos, anticonvulsivos y antidepresivos. AINEs son usados en diferentes entidades de dolor lumbar demostrando una ventaja sobre placebo17 .Opiáceas
Aunque opiáceos tienen un uso común en dolor crónico, hay débil evidencia para el uso en el síndrome de espalda fallida y se tiene que tener en consideración el riesgo de causar dependencia y el trastorno por consumo de sustancias. Por lo tanto, el uso suele ser un tratamiento de último recurso.Anticonvulsivos y antidepresivos
Anticonvulsivos y antidepresivos demuestran resultados prometedores en estudios iniciales, pero faltan los datos sobre la eficacia a largo plazo.8,18 Por otro lado, terapia física y rehabilitación forma parte del tratamiento conservador. Se tiene que concentrar en desarrollar tolerancia, neuroadaptación y acondicionamiento bajo la dirección de un fisioterapeuta que conoce la patología del paciente, su fuerza y sus limitaciones.Terapia cognitivo-conductual u otra terapia psiquiátrica
Terapia cognitivo-conductual u otra terapia psiquiátrica puede mejorar el resultado del tratamiento del síndrome de espalda fallida .19 Existen pocos estudios sobre el tratamiento cconservador y los resultados suelen ser contradictorios.18Tratamiento quirúrgico o invasivo.
El tratamiento invasivo depende de la etiología del paciente y de los hallazgos diagnósticos.Terapias unidad del dolor
En el caso de artropatía de la articulación facetaría, se suele usar procedimientos como bloqueos facetarios o ablación por radiofrecuencia. Si fibrosis epidural contribuye al síndrome de espalda fallida , se usa la fibrinolisis.20 Inyección epidural de esteroides puede ser efectivo para síndrome de espalda fallida en relación con fibrosis epidural, disrupción discal y estenosis espinal pero demuestra débil evidencia.8,20 (puede ver estas técnicas en https://www.doctorpescador.es/bloqueo-facetario/) Terapias neurmoduladoras como la estimulación de la médula espinal (SCS) donde se implanta un dispositivo estimulante para mediar el dolor que siente el paciente tiene fuerte evidencia de superioridad sobre tratamiento conservador y operaciones repetitivas.21 Al mismo tiempo, en el 40% de los casos fallan con este tipo de tratamientos.22Terapias quirúrgicas
Por último, operar de nuevo puede ser útil para pacientes con una patología identificada, que la intervención puede resolver. Se tiene que estar consciente sobre el hecho que el resultado de re-operaciones suele ser inferior y con una morbididad más alta en comparación con SCS. En casos con una alteración del intestino o de la vejiga, una debilidad motora o un déficit neuronal la operación puede ser urgente.1,20 Si quiere seguir leyendo sobre este tipo de patologías puede hacerlo en el siguiente link https://traumatologosalamanca.com/cirugia-de-columna/SI TE DUELE LA ESPALDA CONSULTENOS, CUIDAMOS SU ESPALDA CUIDAMOS DE TI.
#herniadiscal #traumatología # Salamanca #Zamora #cirugíadecolumna #complicaciones #sindromedeespaldafallida #nopuedocaminar #artrodesislumbar #cirugíadeespalda #dolordeespalda.Bibliografía
- Baber Z, Erdek MA. Failed back surgery syndrome: current perspectives. J Pain Res 2016;9:979-987. DOI: 10.2147/JPR.S92776.
- Hoy D, March L, Brooks P, et al. The global burden of low back pain: estimates from the Global Burden of Disease 2010 study. Ann Rheum Dis 2014;73(6):968-74. DOI: 10.1136/annrheumdis-2013-204428.
- Smith M, Davis MA, Stano M, Whedon JM. Aging baby boomers and the rising cost of chronic back pain: secular trend analysis of longitudinal Medical Expenditures Panel Survey data for years 2000 to 2007. J Manipulative Physiol Ther 2013;36(1):2-11. DOI: 10.1016/j.jmpt.2012.12.001.
- Rajaee SS, Bae HW, Kanim LE, Delamarter RB. Spinal fusion in the United States: analysis of trends from 1998 to 2008. Spine (Phila Pa 1976) 2012;37(1):67-76. DOI: 10.1097/BRS.0b013e31820cccfb.
- Sebaaly A, Lahoud MJ, Rizkallah M, Kreichati G, Kharrat K. Etiology, Evaluation, and Treatment of Failed Back Surgery Syndrome. Asian Spine J 2018;12(3):574-585. DOI: 10.4184/asj.2018.12.3.574.
- Clancy C, Quinn A, Wilson F. The aetiologies of Failed Back Surgery Syndrome: A systematic review. J Back Musculoskelet Rehabil 2017;30(3):395-402. DOI: 10.3233/BMR-150318.
- Carragee EJ, Alamin TF, Miller JL, Carragee JM. Discographic, MRI and psychosocial determinants of low back pain disability and remission: a prospective study in subjects with benign persistent back pain. Spine J 2005;5(1):24-35. DOI: 10.1016/j.spinee.2004.05.250.
- Chan CW, Peng P. Failed back surgery syndrome. Pain Med 2011;12(4):577-606. (In eng). DOI: 10.1111/j.1526-4637.2011.01089.x.
- Bordoni B, Marelli F. Failed back surgery syndrome: review and new hypotheses. J Pain Res 2016;9:17-22. DOI: 10.2147/JPR.S96754.
- Schofferman J, Reynolds J, Herzog R, Covington E, Dreyfuss P, O'Neill C. Failed back surgery: etiology and diagnostic evaluation. Spine J 2003;3(5):400-3. DOI: 10.1016/s1529-9430(03)00122-0.
- Assaker R, Zairi F. Failed back surgery syndrome: to re-operate or not to re-operate? A retrospective review of patient selection and failures. Neurochirurgie 2015;61 Suppl 1:S77-82. (In eng). DOI: 10.1016/j.neuchi.2014.10.108.
- Babar S, Saifuddin A. MRI of the post-discectomy lumbar spine. Clin Radiol 2002;57(11):969-81. DOI: 10.1053/crad.2002.1071.
- Eun SS, Lee HY, Lee SH, Kim KH, Liu WC. MRI versus CT for the diagnosis of lumbar spinal stenosis. J Neuroradiol 2012;39(2):104-9. DOI: 10.1016/j.neurad.2011.02.008.
- Datta S, Manchikanti L, Falco FJ, et al. Diagnostic utility of selective nerve root blocks in the diagnosis of lumbosacral radicular pain: systematic review and update of current evidence. Pain Physician 2013;16(2 Suppl):SE97-124.
- Cohen SP, Chen Y, Neufeld NJ. Sacroiliac joint pain: a comprehensive review of epidemiology, diagnosis and treatment. Expert Rev Neurother 2013;13(1):99-116. DOI: 10.1586/ern.12.148.
- Daniell JR, Osti OL. Failed Back Surgery Syndrome: A Review Article. Asian Spine J 2018;12(2):372-379. DOI: 10.4184/asj.2018.12.2.372.
- Roelofs PD, Deyo RA, Koes BW, Scholten RJ, van Tulder MW. Nonsteroidal anti-inflammatory drugs for low back pain: an updated Cochrane review. Spine (Phila Pa 1976) 2008;33(16):1766-74. DOI: 10.1097/BRS.0b013e31817e69d3.
- Desai MJ, Nava A, Rigoard P, Shah B, Taylor RS. Optimal medical, rehabilitation and behavioral management in the setting of failed back surgery syndrome. Neurochirurgie 2015;61 Suppl 1:S66-76. DOI: 10.1016/j.neuchi.2014.09.002.
- Sparkes E, Raphael JH, Duarte RV, LeMarchand K, Jackson C, Ashford RL. A systematic literature review of psychological characteristics as determinants of outcome for spinal cord stimulation therapy. Pain 2010;150(2):284-289. (In eng). DOI: 10.1016/j.pain.2010.05.001.
- Hussain A, Erdek M. Interventional pain management for failed back surgery syndrome. Pain Pract 2014;14(1):64-78. DOI: 10.1111/papr.12035.
- North RB, Kidd DH, Farrokhi F, Piantadosi SA. Spinal cord stimulation versus repeated lumbosacral spine surgery for chronic pain: a randomized, controlled trial. Neurosurgery 2005;56(1):98-106; discussion 106-7. DOI: 10.1227/01.neu.0000144839.65524.e0.
- Cameron T. Safety and efficacy of spinal cord stimulation for the treatment of chronic pain: a 20-year literature review. J Neurosurg 2004;100(3 Suppl Spine):254-67. DOI: 10.3171/spi.2004.100.3.0254.
COMPLICACIONES QUIRURGICAS DE LA CIRUGÍA DE HERNIA DISCAL PARTE 2. (LESIONES VASCULARES )
17 febrero 2022Las complicaciones de la cirugía de hernia discal o de la cirugía de columna, no son muy expuestas por los profesionales en el momento de proponer la intervención quirúrgica de una hernia discal. La cirugía de hernia, es una cirugía estándar entre los cirujanos de columna pero no está exenta de complicaciones, que el paciente debe conocer y asumir. Estas complicaciones existen y se cumplen, así que hay que convivir con ellas y aportar a nuestro pacientes soluciones y apoyo ante ellas.
Las complicaciones vasculares en cirugía de columna son infrecuentes, pero potencialmente letales, pudiendo generar graves secuelas y menoscabos.
Las lesiones de los vasos, en este tipo de cirugía, están íntimamente ligadas a la anatomía quirúrgica de las arterias y las venas, muy próximas al raquis en todo su recorrido.
Generalidades de las complicaciones:
La incidencia y prevalencia de estas complicaciones no es bien conocido ya que no se comunican a la comunidad científica de forma regular, ni las sociedades tienen programas de comunicación. Este tipo de lesión puede ser de varias formas, como es la laceración directa, el estiramiento del vaso, con su posible rotura de la intima y producción de trombosis o la torsión del vaso. El daño que genera esta lesión puede ser directo por el sangrado, ocasionando una hemorragia y su consecuente shock o lesión isquémica en un órgano diana como el cerebro. En ocasiones estos daños pueden provocar aneurismas o pseudoaneurismas, así como fístulas vasculares que generan clínica a los días o semanas de la lesión. El tratamiento ideal de la lesión vascular es la reparación, pero en muchas ocasiones prima la vida del paciente, por el importante shock teniendo que ligar el vaso con sus subsiguientes secuelas en el órgano diana. Actualmente están teniendo especial relevancia la radiología intervencionista en la colocación de coil de embolización y stent en laceraciones.COMPLICACIONES EN LA HERNIA DISCAL CERVICAL
Lesiones en vía anterior
La vía anterior es la vía más empleada en la cirugía del cervical, tanto para patología degenerativa como para patología traumática y tumoral. Su vía esta íntimamente ligada a la vaina carotidea, situada posterior al músculo esternocleidomastoideo (ECM). La carótida a igual que la yugular interna puede lacerarse durante la vía por bisturís o tijeras, pudiendo evitarse esta lesión realizando una disección roma o con dedo para separar el ECM y llegar a la fascia prevertebral y los músculos largos del cuello. Otras causas de lesión son la tracción excesiva de los separadores, que pueden disminuir el flujo arterial y por tanto provocar una isquemia cerebral con una hemiplejia como secuela, puede provocarse también un daño de la intima o lesión de una placa de ateroma y generar una trombosis. No olvidar también al finalizar la cirugía, al quitar los separadores un desgarro venoso o arterial por una deficiente separación de los vasos. La incidencia de estas lesiones es < 1% 6,7. Hay pocas lesiones descritas de la carótida, de hecho un estudio de AO Spine sobre 17625 pacientes ,no describieron ninguna lesión, encontrado en la literatura solo 3 casos descritos. Concluyendo la infrecuencia pero siempre a tener en cuenta en el abordaje 8,9. En caso de rotura de la carótida es primordial la reparación arterial para evitar una isquemia o una reparación intervencionista. En caso de rotura de la yugular interna de no poder reparar, la ligadura no genera importantes secuelas, gracias a sus anastomosis. La lesión de la yugular externa es excepcional, se produce en abordajes anteriores muy posterior. Su ligadura es el tratamiento ideal por escasa repercusión. Se han descrito por la separación excesiva de los vasos, pseudoaneurismas de la tiroidea inferior que ocasionaron obstrucción de la vía aérea, de forma diferida. Su tratamiento ideal es el intervencionismo.Lesión de la arteria vertebral :
La lesión de la arteria vertebral (AV) es la más reportada en la literatura por varios estudios. El más reciente, presentado en el 46º Congreso CSRS del 2019 por un estudio multicéntrico de Corea del Sur 11,describe una incidencia de 0,08%, estudiando 15.582 cirugías cervicales, tanto por vía anterior como posterior, presentando 13 lesiones de la AV.Causas de la lesión vascular
El mecanismo lesionar reportado fue 8% por separación excesiva, 7% entorsión en corrección de deformidad, 23% laceración por el uso de fresas de alta velocidad, 31 % mal posición de tornillos que pasa desapercibida en la cirugía y 31 % trayectoria errónea de los tornillos durante la cirugía. La región con más incidencia de lesión fue la región C1-C2 con un 1,35% y C3-C6 con un 0,20% del total de las cirugías en las que se instrumentaron. En esta serie describen un 23% de lesión isquémica cerebral como secuelas. Otros estudios del la sociedad CSRS , sobre 163.324 cirugías, mostraron 111 casos de complicaciones vasculares (incidencia 0,07%). Las técnicas con más lesiones fueron la instrumentación posterior 32,4%, corpectomía anterior 23,4%, 11,7% disección de la región posterior, 9% discectomia anterior y 7,2% vía anterior. Mostraron secuelas neurológicas el 5,5% , exitus el 4,5 % y sin repercusión el 90% 12. Otra revisión de Guan et al 13 describe una incidencia de complicaciones vasculares del 0,18 al 0,5 % de lesiones de AV en la cirugía anterior. Esta cirugía en el 64 % fue para patología degenerativa como la hernia discal, 14% para tumores ,9 % para fracturas y el resto para pseudoartrosis e infecciones. Describen 38 lesiones de la AV, de las que 61 % la causa fue el motor de alta velocidad empleado en discectomía y en corpectomía, el 16% fue fallo de la instrumentación, el 8% separación excesiva de músculos largos y los otros casos son descompresión foraminal y del ligamento común posterior, y disección con bisturí eléctrico. Los niveles donde se producen más lesiones son C5-C6, C4-C5 y corpectomia de C6.Localización de lesiones de la arteria vertebral
Como se puede apreciar por la literatura, las causas fundamentales de la lesión de la AV es el fresado lateral excesivo de las unciformes durante la discectomia o la corpectomia en vía anterior, y mal posición de instrumentación en la vía posterior. La descompresión lateral excesiva se produce por falta de práctica en el fresado, la perdida de línea media vertebral y por anomalías anatómicas de la AV. La mal posición se ha descrito en varias localizaciones, así en la colocación de tonillo en fracturas de ondontoides, se ha descrito un caso con lesión de la vertebral en la parte superior de la odontoides al atravesar la C1, que causo hemorragia subaracnoidea craneal y exitus. El lugar más frecuente de mal posición es el segmento C1-C2 en abordaje posterior, bien en la colocación transarticular C1-C2 o la colocación pedicular de C2 y la masa lateral del C1 14. La colocación de instrumentación en masa lateral en la columna subaxial es otra región de lesión, cuando no se coloca con la angulación adecuada.Tratamiento de la lesión de la arteria vertebral
Los principios de tratamiento, inicialmente es el taponamiento, evitando un shock hemorrágico con agentes hemostáticos. Pero este tratamiento no puede considerarse definitivo por el riesgo de isquemia. Se debe intentar reparar la AV, disecando lateral los músculos largos y la apófisis transversa y liberando la arteria, se debe controlar por encima y debajo de la lesión con clips o cintas elásticas y proceder a la reparación. Hoy en día en múltiples centros, estas reparaciones se hacen por radiología intervencionista. En caso de lesión por instrumentación y no existir la posibilidad de reparación, se debe taponar y dejar el tornillo colocado, no se debe poner instrumentación en el lado contralateral, por el riesgo de una nueva lesión y un desenlace fatal 15.COMPLICACIONES EN LA HERNIA DISCAL LUMBAR
Lesiones en el abordaje anterior :
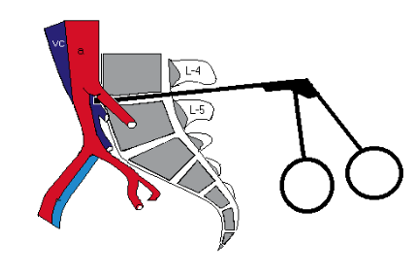
El abordaje anterior se realiza por vía transperitoneal o retroperitoneal izquierdo. Se emplea para tratamiento de los segmentos L4-L5 y L5-S1. Las estructuras vasculares expuestas son la aorta, cava e iliacas y sus ramas. Durante el abordaje hay que identificar y controlar 4 estructuras claves; la vena iliolumbar, la vena ilíaca izquierda, los vasos sacros medios y el tipo de retracción arterial a realizar. La técnica quirúrgica varía según el lugar de bifurcación arterial y venoso. Como norma general, el nivel L4-L5 se debe separar la aorta y la cava de izquierda a derechas, por la dureza y elasticidad de la aorta, ligando las segmentarias, las sacras medias y la vena ileolumbar. El segmento L5-S1 se encuentra en la bifurcación, se debe separar los vasos de forma excéntrica ligando las sacras medias.Tipos de lesiones y localizaciones
La incidencia de complicaciones vasculares con la rotura o laceración no es bien conocida, es infrecuente y las series describen tasas entre el 0%- 18%, con una morbi mortalidad muy baja. Los vasos más lesionados son las venas por su debilidad y falta de elasticidad. La más afectada es la vena iliaca común , seguido de la cava inferior y la vena ileolumbar. Las arterias más afectada es la iliaca izquierda (0- 9%) y la aorta (0,08%). No hay diferencias en cuanto las lesiones y el tipo de abordaje. El nivel con más incidencia de lesión es el L4-L5 por la retracción a realizar. El riesgo aumenta si se implantan prótesis o no, con tasas de 11,5% y 3,2% respectivamente.Tratamiento y actuación ante la lesión vascular
Las actuaciones ante una lesión aguda es el taponamiento y control del sangrado, posteriormente la reparación. En caso de imposibilidad, la ligadura generará secuelas de tipo isquémicas y de retorno venoso. Hay que prestar atención al finalizar la cirugía, revisar un eventual sangrado que hasta que no se retiran los separadores, por la compresión y taponamiento de estos, pueden pasar desapercibidas. Existen casos de lesión diferida por lesión del material protésico, que generaran sangrado o pseudoaneurismas, siendo el intervencionismo un posible tratamiento. Una lesión rara es la trombosis por compresión de los vasos por excesiva retracción, sobre todo de la arteria iliaca común izquierda. Generan isquemia de miembro inferior y suele ser diagnosticado diferidamente. Requiere tratamiento por el cirujano vascular.Lesiones en el abordaje anterolateral.
El abordaje anterolateral se emplea para lesiones del segmento L3-L4 y por encima. Se suele realizar por el lado izquierdo, debido a la visualización directa de la aorta y la protección indirecta de la arteria. Las complicaciones son similares a las expuestas en el abordaje torácico, añadiendo el riesgo de una lesión de la cava o de estructuras como el uréter. También se debe tener precaución con la lesión de la vena ileolumbar, adosada al borde del psoas 18. Se están realizando actualmente, para tratamiento de la deformidad del adulto abordajes lateral directo (XLIF), se han descrito casos de lesión por la instrumentación intervertebral de la aorta 19.Lesiones en el abordaje lumbar posterior .
Es la región anatómica con más reportes de lesiones vasculares, ya que es la región más frecuentemente intervenida y la vía más empleada. Se describen pocos casos de lesiones relacionadas con la instrumentación posterior, siendo la discectomía la causa fundamental, bien simple o asociada a la incorporación de injerto o cajas intersomáticas intervertebral 21,20. La lesión por tornillos transpediculares son infrecuentes, pero se han descrito casos por lesión posterior22. La incidencia de complicaciones vasculares está entre el 0,01% y el 0,05% (4 casos/ 8099 discectomía) , con una alta mortalidad si ocurre entre el 10-65%. Por eso reconocerlo es fundamental para la supervivencia del paciente. El nivel más afecto es el L4-L5 en el 75% de las veces ya que en este nivel los vasos se encuentran a 5mm del cuerpo vertebral, seguido del L5-S1. No hay diferencia entre la discectomía abierta y la endoscópica 23.Tipos y localización de lesión vascular posterior
Las complicaciones vasculares que más se producen por orden de mayor a menor son las fistulas arteriovenosas (66%) 25, la laceración (33%) 26 y los pseudoaneurisma (3%). El vaso más afectado es la arteria iliaca común izquierda (51,2%), vena iliaca común izquierda (23,3%), la cava (9,3%) y la aorta (4,7%). Los instrumentos que más producen estas lesiones son el discotomo y las legras intervertebrales.Factores de riesgos
Los factores de riesgo para que ocurran estas complicaciones son, tener el ligamento anterior roto, patología degenerativa previa, procesos inflamatorios retroperitoneales, que generan fibrosis de los vasos adhiriéndolos al cuerpo vertebral, discectomías amplias y de revisión.Clínica de la lesión vascular posterior
Los síntomas que se producen en la laceración son hipotensión (84,4%), taquicardia (34,4%), disminución hemoglobina (25%) , hemorragia activa visible (43,8%), dolor abdominal (15,6%), masa abdominal ( 6,3%) y distensión abdominal (18,8%). En ocasiones se puede identificar en el discotomo grasa retroperitoneal o tejido visceral, que puede hacernos sospechar la lesión. Las manifestaciones en la fistula son soplo audible (40,7%), dolor abdominal (33.3%), masa abdominal (14,8%) y signos de fallo cardiaco (14,8%) .Diagnóstico de la lesión vascular
Las lesiones vasculares pueden se agudas y emergentes o diferidas, tanto en el postoperatorio inmediato, como a los meses de la cirugía. Ante una lesión aguda lo importante es reconocer la lesión, por los síntomas, si se confirma comenzar rápidamente con el tratamiento. Podemos identificar la lesión por la visualización del sangrado intraoperatorio, pero esto ocurre sólo en el 43% de los casos. Si no es así, se debe recurrir a pruebas de imagen urgentes como la ecografía intraoperatoria o el TAC.Tratamiento de la lesión vascular posterior
El tratamiento se debe comenzar con el tratamiento del shock, con fluidoterapia y aporte sanguíneo. Cierre de la herida, voltear al paciente en decúbito supino y comenzar la laparotomía exploratoria para poder reparar la lesión . Este es el tratamiento gold estándar en pacientes inestables. Se han descrito en centros de referencia, tratamientos intervencionistas emergentes con balón cercano a la lesión, para controlar el sangrado y la reparación posterior con endoprótesis 27. En caso de pacientes estables o en lesiones diferidas el tratamiento reparador se debe realizar por radiología intervencionista 28, 29.Prevención de la lesión vascular
Los consejos para evitar esta lesión en la discectomía es la prevención. Sólo extraer los fragmentos de disco sueltos en el canal, al abrir el disco con el bisturí, sólo introducirlo 4-5 mm o introducir el discotomo sólo entre 2,5 -4 cm dentro del disco. Si quiere seguir leyendo sobre este tipo de patologías puede hacerlo en el siguiente link https://traumatologosalamanca.com/cirugia-de-columna/ o sobre la hernia discal en https://www.doctorpescador.es/hernia-discal-lumbar/SI TIENES HERNIA DISCAL Y TE DUELE LA ESPALDA CONSULTENOS, CUIDAMOS TU ESPALDA, CUIDAMOS DE TI.
#herniadiscal #traumatología # Salamanca #Zamora #Cirugíadecolumna #complicaciones.BIBLIOGRAFIA
- Netter FH. Atlas de Anatomia Humana. Masson. East Hanover , New Jersey; 2001.
- Rouviere, Henri; Delmas A. Anatomía Humana. Descritiva , Topografía y Funcional. 15a. (Masson, ed.). Paris; 2002.
- Frati P, Carbone I, Pugnetti P, Busardo FP, Fineschi V. Iatrogenic left common iliac artery and vein perforation during lumbar discectomy : A fatal case. 2019;246(2015):7-11. doi:10.1016/j.forsciint.2014.11.006
- Inamasu J, Guiot BH. Review Article Vascular injury and complication in neurosurgical spine surgery. 2006:375-387. doi:10.1007/s00701-005-0669-1
- Epstein NE, Epstein NE, Hospital NYUW, Neuroscience NYUW. Surgical Neurology International A Review of Complication Rates for Anterior Cervical Diskectomy and Fusion ( ACDF ). 2019;10(100):3-10. doi:10.25259/SNI-191-2019
- Baran Ş, Yüksel V, Hüseyin S, Güçlü O, Canbaz S. Ruptured Internal Carotid Artery Pseudoaneurysm 10 Years after Cervical Spine Surgery. 2019;35(2):111-113.
- Inamasu J, Guiot BH. Iatrogenic carotid artery injury in neurosurgery. 2005:239-247. doi:10.1007/s10143-005-0412-7
- Alimi M, Boukebir MA, Berlin CD, et al. Carotid Artery Injury in Anterior Cervical Spine Surgery : Multicenter Cohort Study and Literature Review. 2017;7:71-75. doi:10.1177/2192568216688192
- Du Y, Duan W, Chen Z, Wu H, Jian F. Carotid Artery-Related Perioperative Stroke Following Anterior Cervical Spine Surgery : A Series of 3 Cases and Literature Review X Wan-Ru. J Stroke Cerebrovasc Dis. 2019;28(2):458-463. doi:10.1016/j.jstrokecerebrovasdis.2018.10.024
- Peng CW, Chou BT, Bendo JA, Spivak JM. Vertebral artery injury in cervical spine surgery : anatomical considerations , management , and preventive measures. Spine J. 2019;9(1):70-76. doi:10.1016/j.spinee.2008.03.006
- Lee C, Hong JT, Kang DH, et al. Epidemiology of Iatrogenic Vertebral Artery Injury in Cervical Spine Surgery: 21 Multicenter Studies. World Neurosurg. 2019;126:e1050-e1054. doi:10.1016/j.wneu.2019.03.042
- Lunardini DJ, Eskander MS, Even JL, et al. Vertebral artery injuries in cervical spine surgery. Spine J. 2019;14(8):1520-1525. doi:10.1016/j.spinee.2013.09.016
- Guan Q, Chen L, Long Y, Xiang Z. Literature Review Iatrogenic Vertebral Artery Injury During Anterior Cervical Spine Surgery : A Systematic. World Neurosurg. 2019;106:715-722. doi:10.1016/j.wneu.2017.07.027
- Arslan D, Asim M, Govsa F, Kitis O. Surgicoanatomical aspect in vascular variations of the V3 segment of vertebral artery as a risk factor for C1 instrumentation. J Clin Neurosci. 2019;68:243-249. doi:10.1016/j.jocn.2019.07.032
- Belykh E, Xu DS, Yağmurlu K, et al. Repair of V2 Vertebral Artery Injuries Sustained During Anterior Cervical Diskectomy. World Neurosurg. 2017;105:796-804. doi:10.1016/j.wneu.2017.05.154
- Bydon A, Sciubba DM, Wolinsky J, Gokaslan ZL. Incidence and Clinical Significance of Vascular Encroachment Resulting from freehand placement of pedicle screwa in the thoracic and lumbar spine. Analysis of 6816 consecutive screws. Spine J.2014;39(8):683-687. doi:10.1097/BRS.0000000000000221
- Mirza AK, Ali M, Naylor RM, et al. Management of major vascular injury during pedicle screw instrumentation of thoracolumbar spine. Clin Neurol Neurosurg. 2019;163(October 2017):53-59. doi:10.1016/j.clineuro.2017.10.011
- Davis M, Jenkins S, Bordes S, et al. Iliolumbar Vein: Anatomy and Surgical Importance During Lateral Transpsoas and Oblique Approaches to Lumbar Spine. World Neurosurg. 2019;128:e768-e772. doi:10.1016/j.wneu.2019.04.252
- Safaee MM, Zarkowsky D, Eichler CM, Pekmezci M, Clark AJ. Management of aortic injury during minimally invasive lateral lumbar interbody fusion. Eur Spine J. 2018;27(s3):538-543. doi:10.1007/s00586-018-5620-2
- Jung HS, Kim DJ, Kim HS, Lee HK, Jin S, Choi N. Vascular Complications Related to Posterior Lumbar Disc Surgery. 2017;33(4).
- Postacchini R, Cinotti G, Postacchini F. Injury to major abdominal vessels during posterior lumbar interbody fusion . A case report and review of the literature. Spine J. 2019;13(1):e7-e11. doi:10.1016/j.spinee.2012.11.016
- Liu L, Li N, Wang Q, et al. Iatrogenic Lumbar Artery Injury in Spine Surgery: A Literature Review. World Neurosurg. 2019;122:266-271. doi:10.1016/j.wneu.2018.10.219
- Hasan GA, Raheem HQ, Yuser A, Al-naser LM, Sheta RA. Vascular injury in tubular lumbar microdiscectomy , case report and literature review. 2019. doi:10.1177/2050313X19851695
- Umeda A, Saeki N, Nakao M, Kawamoto M. Abdominal Aortic Injury During Vertebroplasty. 2015;40(7):1-3. doi:10.1097/BRS.0000000000000780
- Yan G, Li H, Yang G, Bhetuwal A, Liu J, Li Y. Iatrogenic arteriovenous fistula of the iliac artery after lumbar discectomy surgery : a systematic review of the last 18 years. 2019;9(6):1163-1175. doi:10.21037/qims.2019.05.12
- Jin SC, Park SW, Cho DS. Management of Proximal Iliac Artery Injury during Lumbar Discectomy with Stent Graft. 2012:227-229.
- Olcay A, Keskin K, Eren F. Iliac artery perforation and treatment during lumbar disc surgery by simple balloon tamponade. 2013;22:350-352. doi:10.1007/s00586-012-2436-3
- Moutinho M. Complete Disruption of The Iliac Vessels During Spinal Surgery With Delayed Presentation. EJVES Short Reports. 2019;43:33-36. doi:10.1016/j.ejvssr.2019.04.008
- Zitteren M Van, Fan B, Lohle PN, et al. A Shift Toward Endovascular Repair for Vascular Complications in Lumbar Disc Surgery During the Last Decade. Ann Vasc Surg. 2019;27(6):810-819. doi:10.1016/j.avsg.2012.07.019
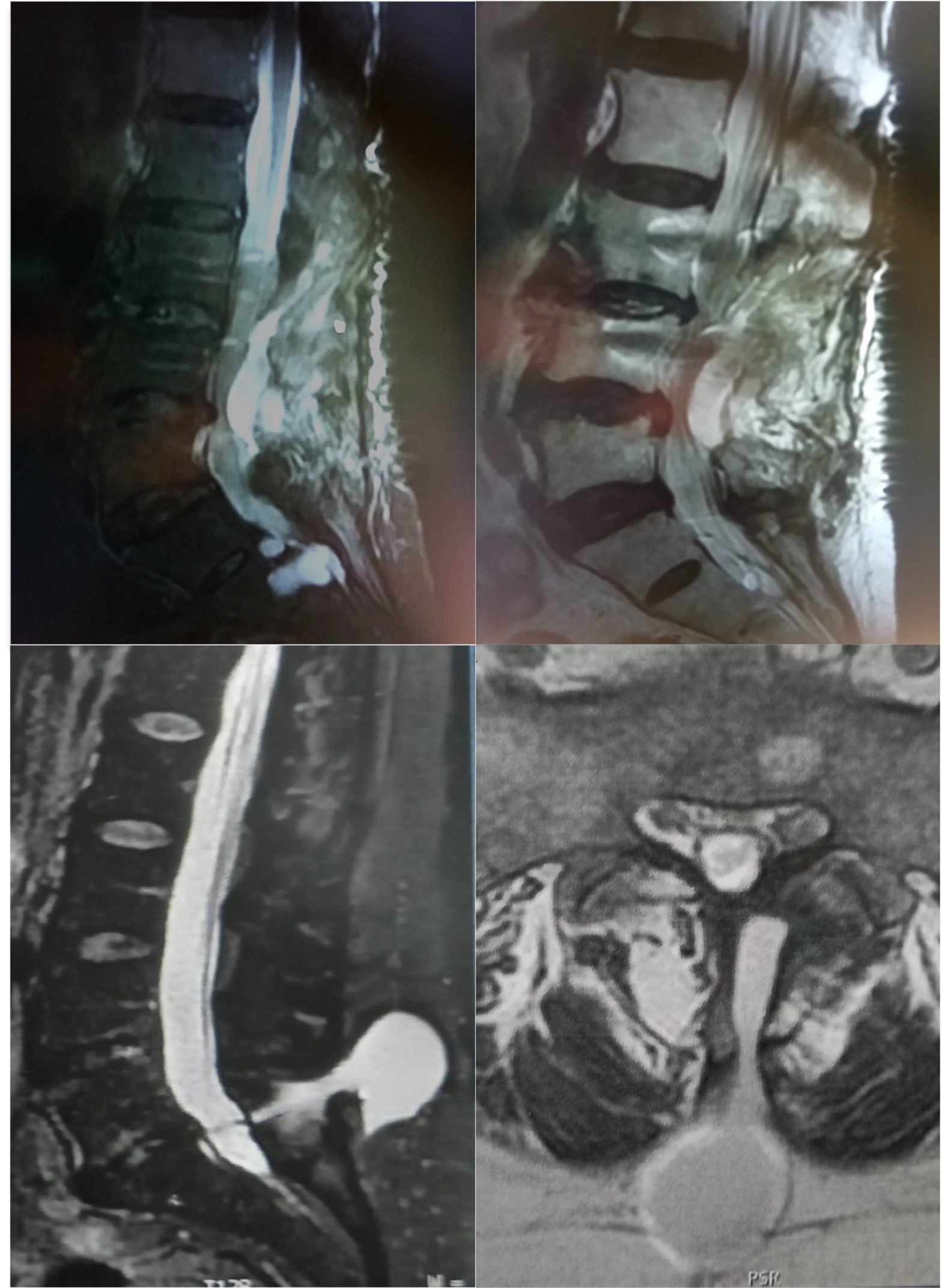
COMPLICACIONES QUIRURGICAS DE LA CIRUGÍA DE HERNIA DISCAL PARTE 1. (ROTURA DURAL, FISTULA DE LCR, DEFICIT NEUROLÓGICO, MENINGITIS, LESIÓN CEREBRAL)
17 enero 2022Las complicaciones de la cirugía de hernia discal o de la cirugía de columna, no son muy expuestas por los profesionales en el momento de proponer la intervención quirúrgica de una hernia discal. La cirugía de hernia, es una cirugía estándar entre los cirujanos de columna pero no está exenta de complicaciones, que el paciente debe conocer y asumir. Estas complicaciones existen y se cumplen, así que hay que convivir con ellas y aportar a nuestro pacientes soluciones y apoyo ante ellas.
La tasa de complicaciones globales de la cirugía de la hernia de disco está entorno al 12%, suponiendo la rotura dural la complicación más frecuente y común de la discectomía, que se encuentra en un 3-7%. Otras complicaciones de menor frecuencia son el hematoma 0,5%, déficit neurológico 1,3-2,6%, infección herida y seroma 2,1%, meningitis 0,1%. Existen un 8,3% de pacientes que presentan malos resultados de la cirugía sin tener complicaciones (Sd. de espalda fallida o postlaminectomía).
Reseñar que los profesionales que no explican las complicaciones, o comentan a sus pacientes que ellos nos las tienen, no es ético por su parte, ya que todo cirujano las tiene y debe asumirlas y afrontarlas.
LA ROTURA DURAL:
La rotura dural es una de las complicaciones más frecuente y común de la cirugía lumbar , siendo su incidencia muy variable en la literatura científica, rondando entre el 3-7%. Consiste en la rotura de la membrana duramadre que envuelve los nervios de la cola de caballo en la región lumbar. Tras la rotura se produce salida de líquido cefalorraquídeo. Las localizaciones más frecuentes son la zona caudal a la lámina superior, zona craneal de la lámina inferior, zona del disco y zona medial de la faceta. También es más frecuente en mujeres y con la edad avanzada.CÓMO SE PRODUCE
Su mecanismo de producción son múltiples, desde lesión a al abrir el ligamento amarillo, al realizar la laminectomía , al movilizar los nervios para localizar la hernia y al extraerla. No siendo fácil identificar cuando sucede la incidencia, si siendo importante darse cuenta de su producción e intentar repararla antes del cierre.TRATAMIENTO
Hay varios métodos de tratamiento, el cierre directo con sutura , con materiales sintéticos tipo pegamento o parches autoadherentes (Tissucol, Duragen, Surgicel…) o combinación de ambos, y en algunos casos se tratan sin reparar con cierre directo de la herida. Las diferentes técnicas son validas no habiendo diferencia entre los diferentes métodos, según las características de la rotura, bien cada una por separado o juntas. No hay diferencia entre usar sutura primaria, selladores o combinada, en cuanto a reintervención por fistula, tiempo hospitalario , tiempo quirúrgico y resultados clínicos.CÓMO COMPROBAMOS EL CIERRE DURAL
Tras la reparación se procede a la comprobación de la estanqueidad por visión directa y por maniobra de Valsalva ( maniobra anestésica que consiste en aumento de presión positiva en el tórax para valorar la salida de LCR en zona de la rotura), esta maniobra se realiza siempre no siendo posible la finalización de la cirugía sin esta comprobación.QUÉ HACER EN EL POSTOPERATORIO
El postoperatorio inmediato es normal la cefalea postural por la perdida de LCR durante la cirugía hasta en un 25%. Las medidas posturales postquirúrgicas son variables algunos autores mantienen un reposo de varios días en cama y otros permiten la movilización inmediata. Los últimos estudios demuestran que mantener más de 24h aumenta la tasa de complicaciones.APARICIÓN DE FISTULA DE LCR
La reparación de dural tiene una tasa de fracaso del 5-9%, por la perdida de resistencia de la duramadre por la sutura o fracaso del sellado , y al aumentar la presión del LCR al producirse, pudiendo generar re rotura y fuga de LCR ( fistula de LCR). Ante la aparición de fistula de LCR se recomienda reposo absoluto en cama siendo mandatorio la reintervención si fracasa el reposo absoluto en cama en 5-7 días. Otras técnicas antes de la cirugía pueden ser validas como el parche de sangre, toma de cafeína, sellantes percutáneos… La reintervención por fistula de LCR plantea los mismos procedimientos técnicos que ante una rotura dural. Los resultados a largo plazo de los pacientes intervenidos de fistula y rotura dural son iguales que los pacientes que no han sufrido esta complicación. En ocasiones puede haber fistula de LCR, con cierre completo de la herida. En estos casos se forma un pseudomeningocele. Que debe ser tratado como una fistula.DÉFICIT NEUROLÓGICO:
Las lesiones neurológicas es parte de las complicaciones en la cirugía lumbar ocurren entorno al 3-4%, suponiendo la paresia de L5 una de las más frecuentes. Hay dos tipo de causas de paresia, las que pueden ser reparadas en la reintervención y las que no. Las que pueden ser reparadas, tenemos el hematoma a tensión (0.50%), compresión por restos discales, restos de fragmentos óseos… y las que no, que son por movilización nerviosa para localizar la hernia y extraerla (sobre todo en hernias grandes), la tracción y contusión nerviosa. Ante una parálisis aguda se aconseja revisar la cirugía lo más rápidamente , para evitar que la lesión se haga irreversibles y mejore el pronóstico. Debiendo realizarse antes de 12h La solicitud de pruebas de imagen previa no se considera primordial, por la demora de la intervención y encontrándose en muchas ocasiones distorsionadas por la cirugía previa. Pero si una resonancia urgente debe plantearse en esta situaciones, sino retrasa el tratamiento quirúrgico. La recuperación nerviosa posteriormente es muy variable e impredecible incluso en causas reparables, pero siendo mandatario internar la revisión quirúrgica en el menor tiempo posible, para obtener un mejor resultado.MENINGITIS:
La meningitis es una complicación muy rara, solo 1 de cada 1000 pacientes intervenidos de patología lumbar. Pocos casos descritos tras fistula de LCR se describen en la literatura científica y los descritos suceden en fistulas mantenidas durante 1 mes. Cursan con fiebre, signos meníngeos (rigidez de nuca) y estupor. Es de vital importancia su diagnóstico precoz y su tratamiento inmediato. El tratamiento consiste en soporte vital avanzado ( ingreso en UVI) , antibioterapia de amplio espectro y si estamos ante una fistula de LCR reintervención para el cierre de ella.PATOLOGÍA CEREBRAL:
Las complicaciones cerebrales tras la cirugía lumbar están descritas pero son excepcionales y muy raras. Con una incidencia menor que la meningitis. Consisten en hemorragias cerebrales , su mecanismo de producción es desconocido y sólo teorías de una tracción de las meninges se ha descrito. Su síntomas consisten en clínica neurológica focal, estupor , cefalea…Su diagnóstico se fundamenta en la realización de un TAC y la exploración clínica. Si quiere seguir leyendo sobre este tipo de patologías puede hacerlo en el siguiente link https://traumatologosalamanca.com/cirugia-de-columna/ o sobre la hernia discal en https://www.doctorpescador.es/hernia-discal-lumbar/SI TIENES HERNIA DISCAL Y TE DUELE LA ESPALDA CONSULTENOS, CUIDAMOS TU ESPALDA, CUIDAMOS DE TI.
#herniadiscal #traumatología # Salamanca #Zamora #Cirugíadecolumna #complicaciones.BIBLIOGRAFÍA
- Incidental duraltear in lumbar spinal decompression and discectomy: analysis of a nationwide database. Yoshihara H, YoneokaD.ArchOrthop Trauma Surg. 2013 Nov;133(11):1501-8. doi: 10.1007/s00402-013-1843-1. Epub 2013 Sep 4.
- Lumbar microdiscectomy complication rates: a systematic review and meta-analysis.Shriver MF, Xie JJ, Tye EY, Rosenbaum BP, Kshettry VR, Benzel EC, Mroz TE. 2015 Oct;39(4):E6. doi: 10.3171/2015.7.FOCUS15281.
- Incidental durotomy during lumbar spine surgery: risk factors and anatomic locations: clinical article. Takahashi Y, Sato T, Hyodo H, Kawamata T, Takahashi E, Miyatake N, Neurosurg Spine. 2013 Feb;18(2):165-9. doi: 10.3171/2012.10.SPINE12271. Epub 2012 Nov 30.
- Microdiscectomy for lumbosacral disc herniation and frequency of failed disc surgery.Shamim MS, Parekh MA, Bari ME, Enam SA, KhursheedF.WorldNeurosurg. 2010 Dec;74(6):611-6. doi: 10.1016/j.wneu.2010.06.016.
- Intra- and postoperative complications in lumbar disc surgery. Stolke D, Sollmann WP, Seifert V. Spine (Phila Pa 1976). 1989 Jan;14(1):56-9.PMID: 2913669
- Dural lesions in decompression for lumbar spinal stenosis: incidence, risk factors and effect on outcome. Strömqvist F, Jönsson B, Strömqvist B; Swedish Society of Spinal Surgeons. Eur Spine J. 2012 May;21(5):825-8. doi: 10.1007/s00586-011-2101-2. Epub 2011 Dec 7.PMID:22146791
- Primary dural repair during minimally invasive microdiscectomy using standard operating room instruments.Chou D, Wang VY, Khan AS.Neurosurgery. 2009 May;64(5 Suppl 2):356-8; discussion 358-9. Doi.10.1227/01.NEU.0000338942.11337.DA.
- Management of Incidental Dural Tear During Lumbar Spine Surgery. To Suture or Not to Suture?Kamenova M, Leu S, Mariani L, Schaeren S, Soleman J.World Neurosurg. 2016 Mar;87:455-62. doi: 10.1016/j.wneu.2015.11.045. Epub 2015 Dec 14.
- Dural tears in primary decompressive lumbar surgery. Is primary repair necessary for a good outcome?. Grannum S et al. Eur Spine J. (2014)
- The use of surgical sealants in the repair of dural tears during non-instrumented spinal surgery. Eur Spine Surg. 2014; 23: 1761-66. Miscusi M1, Polli FM, Forcato S, Coman MA, Ricciardi L, Ramieri A, Raco A.
- The intra- and postoperative management of accidental durotomy in lumbar spine surgery: results of a German survey. Clajus C, Stockhammer F, Rohde V. Acta Neurochir (Wien). 2015 Mar;157(3):525-30. doi: 10.1007/s00701-014-2325-0. Epub 2015 Jan 11.
- Pilot study of perioperative accidental durotomy: does the period of postoperative bed rest reduce the incidence of complication?Low JC, von Niederhäusern B, Rutherford SA, King AT.Br J Neurosurg. 2013 Dec;27(6):800-2. doi: 10.3109/02688697.2013.798858. Epub 2013 Jun 3.PMID:23724795
- Dural tears in primary decompressive lumbar surgery. Is primary repair necessary for a good outcome?. Grannum S et al. Eur Spine J. (2014)
- Incidental durotomy in lumbar spine surgery: incidence and management. Tafazal SI et al. Eur spine J, 2005: 14:287-290
- The intra- and postoperative management of accidental durotomy in lumbar spine surgery: results of a German survey. Clajus C, Stockhammer F, Rohde V. Acta Neurochir (Wien). 2015 Mar;157(3):525-30. doi: 10.1007/s00701-014-2325-0. Epub 2015 Jan 11.
- Postoperative management of incidental durotomy in minimally invasive lumbar spinal surgery.Than KD, Wang AC, Etame AB, La Marca F, Park P.Minim Invasive Neurosurg. 2008 Oct;51(5):263-6. doi: 10.1055/s-0028-1082313. Epub 2008 Oct 14.
- Management of incidental durotomy without mandatory bed rest. A retrospective review of 20 cases. Hodges SD, Humphreys SC, Eck JC, Covington LA.Spine (Phila Pa 1976). 1999 Oct 1;24(19):2062-4.
- Dural tears in primary decompressive lumbar surgery. Is primary repair necessary for a good outcome?. Grannum S et al. Eur Spine J. (2014)
- Postoperative management protocol for incidental dural tears during degenerative lumbar spine surgery: a review of 3,183 consecutive degenerative lumbar cases.Khan MH, Rihn J, Steele G, Davis R, Donaldson WF 3rd, Kang JD, Lee JY.Spine (Phila Pa 1976). 2006 Oct 15;31(22):2609-13.
- The intra- and postoperative management of accidental durotomy in lumbar spine surgery: results of a German survey. Clajus C, Stockhammer F, Rohde V. Acta Neurochir (Wien). 2015 Mar;157(3):525-30. doi: 10.1007/s00701-014-2325-0. Epub 2015 Jan 11.
- Conservative treatment of CSF leakage after lumbosacral operations. Waisman M, Schweppe Y. Harefuah. 1991 Feb 1;120(3):129-30.
- Postoperative cerebrospinal fluid leakage after lumbar spine operations. Conservative treatment.Waisman M, Schweppe Y. Spine (Phila Pa 1976). 1991 Jan;16(1):52-3
- Incidental durotomy after spinal surgery: a prospective study in an academic institution. McMahon P, Dididze M, Levi AD. J Neurosurg Spine. 2012 Jul;17(1):30-6. doi: 10.3171/2012.3.SPINE11939. Epub 2012 Apr 27.PMID:22540168
- The use of surgical sealants in the repair of dural tears during non-instrumented spinal surgery. Eur Spine Surg. 2014; 23: 1761-66. Miscusi M1, Polli FM, Forcato S, Coman MA, Ricciardi L, Ramieri A, Raco A.
- Evaluation and treatment of dural tears in lumbar spine surgery: a review. Bosacco SJ1, Gardner MJ, Guille JT. Clin Orthop Relat Res. 2001 Aug;(389):238-47.
- Treatment of cerebrospinal fluid leak after spine surgery. Fang Z, Tian R, Jia YT, Xu TT, Liu Y.Chin J Traumatol. 2017 Apr;20(2):81-83. doi: 10.1016/j.cjtee.2016.12.002. Epub 2017 Feb 24. Review.
- Cerebrospinal fluid leaks following spinal surgery: use of fat grafts for prevention and repair. Technical note. Black P. J Neurosurg. 2002 Mar;96(2 Suppl):250-2.
- Incidental durotomy in spine surgery. Cammisa FP Jr, Girardi FP, Sangani PK, Parvataneni HK, Cadag S, Sandhu HS. Spine (Phila Pa 1976). 2000 Oct 15;25(20):2663-7.
- Dural tears secondary to operations on the lumbar spine. Management and results after a two-year-minimum follow-up of eighty-eight patients. Wang JC, Bohlman HH, Riew KD. J Bone Joint Surg Am. 1998 Dec;80(12):1728-32.
- SPORT:Does incidental durotomy affect longterm outcomes in cases of spinal stenosis?Desai A1, Ball PA, Bekelis K, Lurie J, Mirza SK, Tosteson TD, Weinstein JN. 2015 Mar;76 Suppl 1:S57-63; discussion S63. doi: 10.1227/01.neu.0000462078.58454.f4.
- Incidence of postoperative symptomatic epidural hematoma in spinal decompression surgery.Aono H, Ohwada T, Hosono N, Tobimatsu H, Ariga K, Fuji T, Iwasaki M.J Neurosurg Spine. 2011 Aug;15(2):202-5. doi: 10.3171/2011.3.SPINE10716. Epub 2011 May 6
- Surgical management of spinal epidural hematoma: relationship between surgical timing and neurological outcome. JNJS 1995
- Iatrogenic neurologic deficit after lumbar spine surgery: A review.Ghobrial GM, Williams KA Jr, Arnold P, Fehlings M, Harrop JS.Clin Neurol Neurosurg. 2015 Dec;139:76-80. doi: 10.1016/j.clineuro.2015.08.022. Epub 2015 Sep 1. Review.
- Surgical treatment for bacterial meningitis after spinal surgery: A case report.Zhang LM, Ren L, Zhao ZQ, Zhao YR, Zheng YF, Zhou JL.Medicine (Baltimore). 2017 Mar;96(11):e6099. doi: 10.1097/MD.0000000000006099.
- Postoperative meningitis after spinal surgery: a review of 21 cases from 20,178 patients.Lin TY, Chen WJ, Hsieh MK, Lu ML, Tsai TT, Lai PL, Fu TS, Niu CC, Chen LH.BMC Infect Dis. 2014 Apr 23;14:220. doi: 10.1186/1471-2334-14-220.
- Acinetobacter baumanii meningitis: a rare complication of incidental durotomy. deFreitas DJ, McCabe JP.J Spinal Disord Tech. 2004 Apr;17(2):115-6.
- Intracranial subdural hematoma after unintended durotomy during spine surgery. Lu CH, Ho ST, Kong SS, Cherng CH, Wong CS. Can J Anaesth. 2002 Jan;49(1):100-2.PMID:1178233
- Remote cerebellar hemorrhage caused by undetected dural tear after lumbar spinal surgery. Val-Jordán E1, Seral-Moral P2, Novo-González B Rev Esp Cir Ortop Traumatol.2017 Sep 4. pii: S1888-4415(17)30099-1. doi: 10.1016/j.recot.2017.06.006.
- Intracraneal complications after raquis surgery. Rev Esp Cir OrtopTraumatol.2017 Jul 7. pii: S1888-4415(17)30061-9. doi: 10.1016/j.recot.2017.03.005
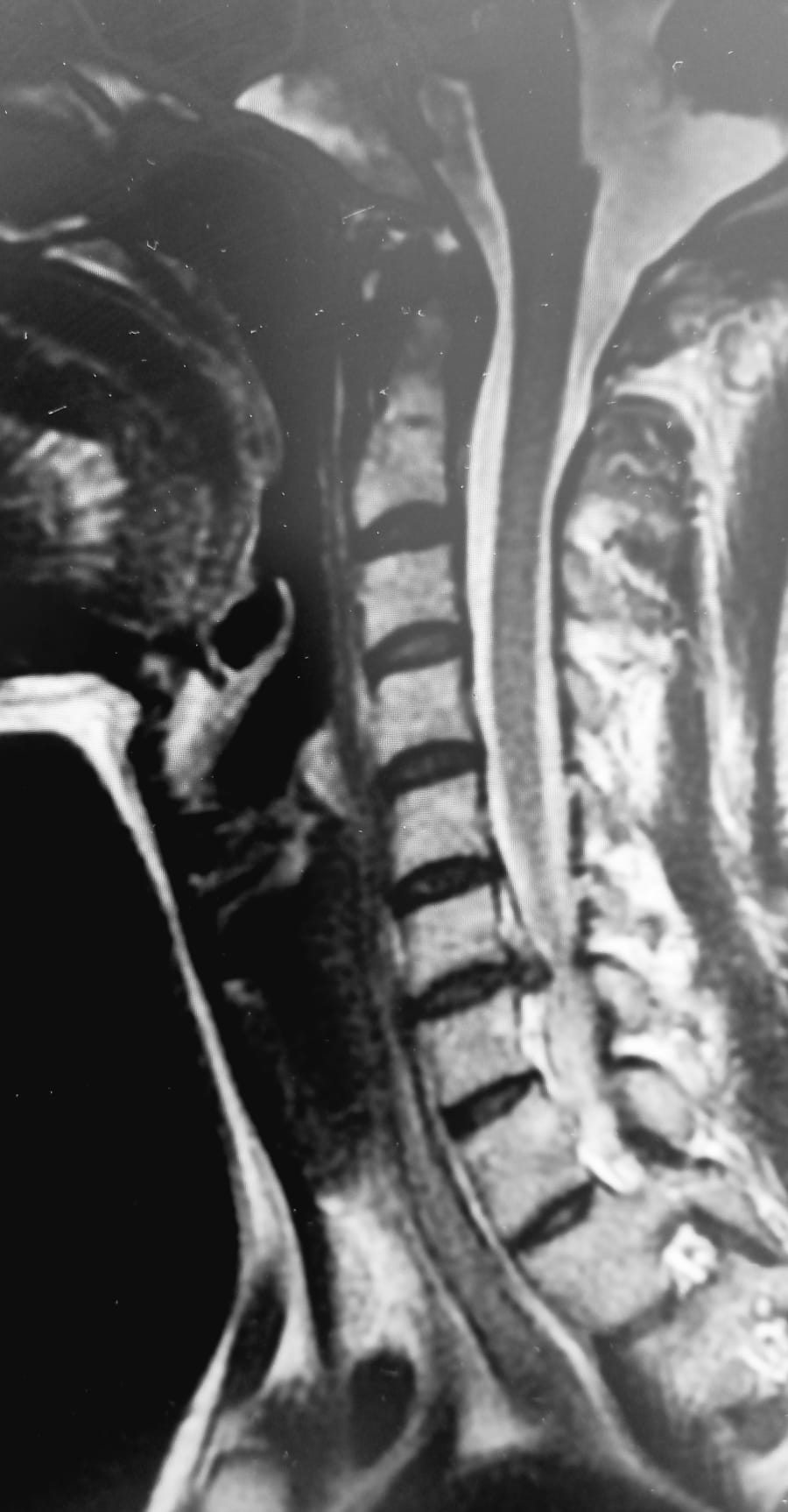
SE TE DUERMEN LAS MANOS, TE HORMIGUEAN, TE QUEMAN, TIENES PARESTESIAS… PUEDEN SER VARIAS CAUSAS, DESCUBRELAS. (HERNIA DISCAL CERVICAL, SINDROME DEL TUNEL DEL CARPO Y NEUROPATIA DEL CUBITAL)
25 diciembre 2021Los hormigueos en las manos es una causa muy frecuente de consulta en traumatología. Este síntoma se denomina parestesias y varias patologías pueden producirlas. Comentamos las más frecuentes la hernia discal cervical, síndrome del túnel del carpo y neuropatía del cubital)
PARESTESIAS EN MIEMBRO SUPERIOR
La parestesia es un fenómeno neurológico producido por un trastorno de la sensibilidad de tipo irritativo que se manifiesta con sensaciones anormales sin estímulo previo, como pérdida de sensibilidad, hormigueo, picor, entumecimiento o quemazón. Existen diferentes síndromes compresivos sobre los nervios que producen esta sintomatologíaHERNIA DISCAL CERVICAL Y LAS PARESTESIAS
La hernia discal cervical es una causa común de radiculopatía cervical, su etiología es multifactorial, encontrando algunos factores de riesgo como género masculino, tabaquismo, cargar peso y distintas ocupaciones manuales. El nivel más afectado es el C5-C6Clínica
La sintomatología surge del pinzamiento o presión que ejerce el material del disco herniado sobre los nervios cervicales. Esta consiste en dolor de brazo que se acompaña de síntomas sensoriales como entumecimiento, hormigueo y debilidad muscular.Diagnóstico
El gold standard para el diagnóstico de la hernia discal cervical es la RMN (Resonancia Magnética Nuclear). También se puede solicitar un EMG para descartar otros síndromes de atrapamiento con sintomatología similar y para conocer el grado de afectación de cada nervioTratamiento
El tratamiento suele ser conservador, basado en el control con medicación y tratamientos no quirúrgicos como la fisioterapia, las infiltraciones o bloqueos .Si la sintomatología no mejora se contemplaría el tratamiento quirúrgico siendo el gold standard la disectomía cervical anterior y la fusión.SINDROME DEL TUNEL DEL CARPO Y LAS PARESTESIAS
El síndrome del túnel del carpo es el síndrome de atrapamiento nervioso más común, es causado por la compresión del nervio mediano en su paso por el canal osteotendinoso situado en la cara anterior de la muñeca (túnel del carpo).Ocurre entre el 0,1 – 10% de la población general , su edad más frecuente es entre 45 y 54 años. Es más frecuente en mujeres.Etiología
Existen algunos factores de riesgo asociados como la diabetes mellitus tipo 1 y 2, el sobrepeso y la obesidad, circunstancias laborales (como el uso abusivo del ordenador), el tabaquismo, el embarazo o el hipotiroidismo. La causa más frecuente es la idiopática (95%).Diagnóstico
El gold standard para el diagnóstico es una detallada historia clínica junto a la exclusión de otras posibles causas. Su clínica es característica y consiste en parestesias y disestesias nocturnas intermitentes en los tres primeros dedos de la mano, que asocian dolor y que pueden evolucionar a debilidad y atrofia de la musculatura tenar como consecuencia de la degeneración axonal. Esta sintomatología puede reflejarse en el antebrazo y llegar hasta el hombro. Existen algunas maniobras para desencadenar y reproducir la sintomatología que se pueden aplicar en el estudio diagnostico cómo los signos de Phalen ,Tinel y Durkan. Además, para completar el diagnóstico y valorar la conducción nerviosa y el grado de afectación se llevan a cabo estudios nuerofisiológicos como el elecotromiograma (EMG) y un estudio de conducción nerviosa (ECN). Los recientes avances técnicos han permitido incorporar a la ultrasonografía como herramienta diagnostica para esta patología.Tratamiento
Existen varias opciones terapéuticas no quirúrgicas. La primera línea en el manejo de esta patología sería la educación del paciente (cambio de hábitos, uso de herramientas ergonómicas…). La terapia laser con infrarrojos ha demostrado cierta eficacia aunque no existe una gran evidencia científica sobre ello. El tratamiento farmacoterápico consistiría en infiltraciones con corticoesteroides aunque tienen una efectividad limitada. El uso de férulas y la manipulación musculoesquelética con masajes, ejercicios y movilización también suponen un beneficio en el manejo de la sintomatología. El tratamiento quirúrgico consiste en la liberación del canal del carpo mediante la resección del ligamento tanular del carpo. Existen distintas técnicas de abordaje como la técnica abierta tradicional, con un abordaje mínimamente invasivo o mediante técnica endoscópica pero no existe suficiente evidencia sobre el mayor beneficio de unas u otras. En este link pueden ver la cirugía https://www.youtube.com/watch?v=MqEncMlI_FM&list=PLOqanlCC9Fwg26SbhX_sgAfSCIQ69F-m9&index=4NEUROPATIA DEL NERVIO CUBITAL EN EL CODO Y LAS PARESTESIAS
El síndrome del túnel cubital es el segundo síndrome de compresión nerviosa periférica más común causado por la comprensión del nervio cubital en el codo, al nivel del epicóndilo medial donde pasa por detrás y por debajo del ligamento de Osborne y la fascia proximal del flexor cubital del carpo.Etiología
Dependiendo de la etiología puede categorizarse como síndrome cubital primario o idiopático y secundario o sintomático. En el síndrome primario no encontramos alteraciones morfológicas e incluye factores de riesgo como la luxación del nervio cubital, la presencia del musculo anconeus epitrochlearis o la hipertrofia o dislocación de la cabeza media del tríceps. La segunda forma es secundaria a deformidades (especialmente tras una fractura distal del humero mal consolidada) como valgo o varo cubital, cambios osteoartróticos con exostosis. También a situaciones de inestabilidad de la articulación del codo como en la artrits reumatoide, con proliferación de la sinovial y la osificación heterotrópica por traumatismos antiguos. Finalmente a lesiones del tejido blando como el lipoma, ganglios, engrosamiento de plexo venoso, quistes o procesos inflamatorios.Clínica
La sintomatología se caracteriza por entumecimiento del quinto y la mitad cubital del cuarto dedo y también por cambios sensoriales en la mitad cubital del brazo. Los pacientes también refieren dolor. Con la progresión de la lesión se produce una degeneración axonal y denervación de los músculos lumbricales intrínsecos que se traducirá en debilidad muscular y falta de precisión en el uso de la mano. Finalmente podría producir una atrofia de los músculos interóseos y del musculo adductor pollicis y la deformidad de la mano en garra.Diagnóstico
Esta descripción sintomatológica resulta esencial en el proceso diagnóstico que se tendrá que acompañar de un examen clínico que incluye:- Palpación del curso del nervio cubital buscando una posible luxación en el surco retrocondileo
- Examen de la movilidad y estabilidad de la articulación del codo
- Examen de déficit motor a través del signo de Froment
- Examen del déficit sensorial
- Tests inespecíficos como el signo de Hoffmann-Tinel o los tests de flexión.
Tratamiento
El tratamiento conservador comenzaría con la educación al paciente asociada con un cambio de hábitos en aquellos casos en los que la sintomatología se ha desarrollado en los últimos 14 días. En caso de que no cedan los síntomas irritativos se podrán aplicar algunas opciones terapéuticas cómo la fijación nocturna del codo con una férula, la infiltración local con corticoides no presenta una mejora sintomática mayor a la fijación con férula y asocia mayores complicaciones. La intervención quirúrgica está indicada en casos de permanencia y progreso del malestar, de déficit sensomotor y atrofia muscular o sí no existe mejora electrofisiológica tras varios meses de tratamiento conservador. Existen varios procedimientos quirúrgicos aceptados- Descompresión in situ o endoscópica, de elección en el síndrome cubital primario
- Descompresión con transposición subcutánea, intramuscular y submuscular, recomendado en deformaciones post traumáticas o degenerativas, subluxaciones del nervio cubital o cuando el nervio está envuelto en tejido cicatrizal.
- Descompresión con epicondilectomía, en aquellos casos donde el cirujano tenga suficiente experiencia y exista una severa deformación del epicondilo medial o una deformidad en valgo).
NEUROPATIA DEL NERVIO CUBITAL EN EL CANAL DE GUYÓN Y LAS PARESTESIAS
Es la compresión del nervio cubital en el canal de Guyón. El canal del Guyón está situado en la zona cubital de la muñeca por el que circulan el nervio y la arteria cubital. La causa no suele ser idiopática, el 80% de las veces suele ser por gangliones o tumores. Otras causas son las alteraciones del hueso ganchoso como las fracturas.Clínica
Hormigueos o entumecimiento de los dedos 4º y 5º, en la zona volar. Disminución de sensibilidad del 5º dedo y la mitad del 4º. Debilidad de la musculatura y déficit sensorial dela cara cubital de la mano.Diagnóstico
La clínica es fundamental para el diagnóstico, es muy importante identificar los músculos y los dermatomos afectados. Lo confirmamos por un electromiograma. (EMG) La resonancia y la ecografía nos sirve para identificar lesiones que ocupan el canal como tumores o gangliones.Tratamiento
El tratamiento conservador consiste en el cambio de hábitos. Las infiltraciones pueden ayudar. Sino el tratamiento quirúrgico de descompresión y reparación de la causa es el tratamiento definitivo Si quiere seguir leyendo sobre otras patologías consulte https://traumatologosalamanca.com/traumatologia-cirugia-ortopedica/SI TE HORMIGUEAN O TE QUEMAN LAS MANOS CONSULTENOS, CUIDAMOS TU ESPALDA Y TUS BRAZOS, CUIDAMOS DE TI
#traumatologo #traumatología #Salamanca #Zamora #herniadiscal #sindromedeltuneldelcarpo #parestesias #neuropaitacubital #hormigueos #quemazon
BIBLIOGRAFIA
- Assmus, H., Antoniadis, G., Bischoff, C., Hoffmann, R., Martini, A. K., Preißler, P., Scheglmann, K., Schwerdtfeger, K., Wessels, K. D., & Wüstner-Hofmann, M. (2011). Cubital Tunnel Syndrome – A Review and Management Guidelines. Central European Neurosurgery, 72(02), 90–98. https://doi.org/10.1055/s-0031-1271800
- Mazas, S., Benzakour, A., Castelain, J. E., Damade, C., Ghailane, S., & Gille, O. (2018). Cervical disc herniation: which surgery? International Orthopaedics, 43(4), 761–766. https://doi.org/10.1007/s00264-018-4221-3
- McCartney, S., Baskerville, R., Blagg, S., & McCartney, D. (2017). Cervical radiculopathy and cervical myelopathy: diagnosis and management in primary care. British Journal of General Practice, 68(666), 44–46. https://doi.org/10.3399/bjgp17x694361
- Padua, L., Coraci, D., Erra, C., Pazzaglia, C., Paolasso, I., Loreti, C., Caliandro, P., & Hobson-Webb, L. D. (2016). Carpal tunnel syndrome: clinical features, diagnosis, and management. The Lancet Neurology, 15(12), 1273–1284. https://doi.org/10.1016/s1474-4422(16)30231-9
- Spies, C. K., Löw, S., Langer, M. F., Hohendorff, B., Müller, L. P., & Unglaub, F. (2017). Der Orthopäde, 46(8), 717–726. https://doi.org/10.1007/s00132-017-3453-z
- Thomson, J. G. (2017). Diagnosis and treatment of carpal tunnel syndrome. The Lancet Neurology, 16(4), 263. https://doi.org/10.1016/s1474-4422(17)30059-5
- Wong, J. J., Côté, P., Quesnele, J. J., Stern, P. J., & Mior, S. A. (2014). The course and prognostic factors of symptomatic cervical disc herniation with radiculopathy: a systematic review of the literature. The Spine Journal, 14(8), 1781–1789. https://doi.org/10.1016/j.spinee.2014.02.032
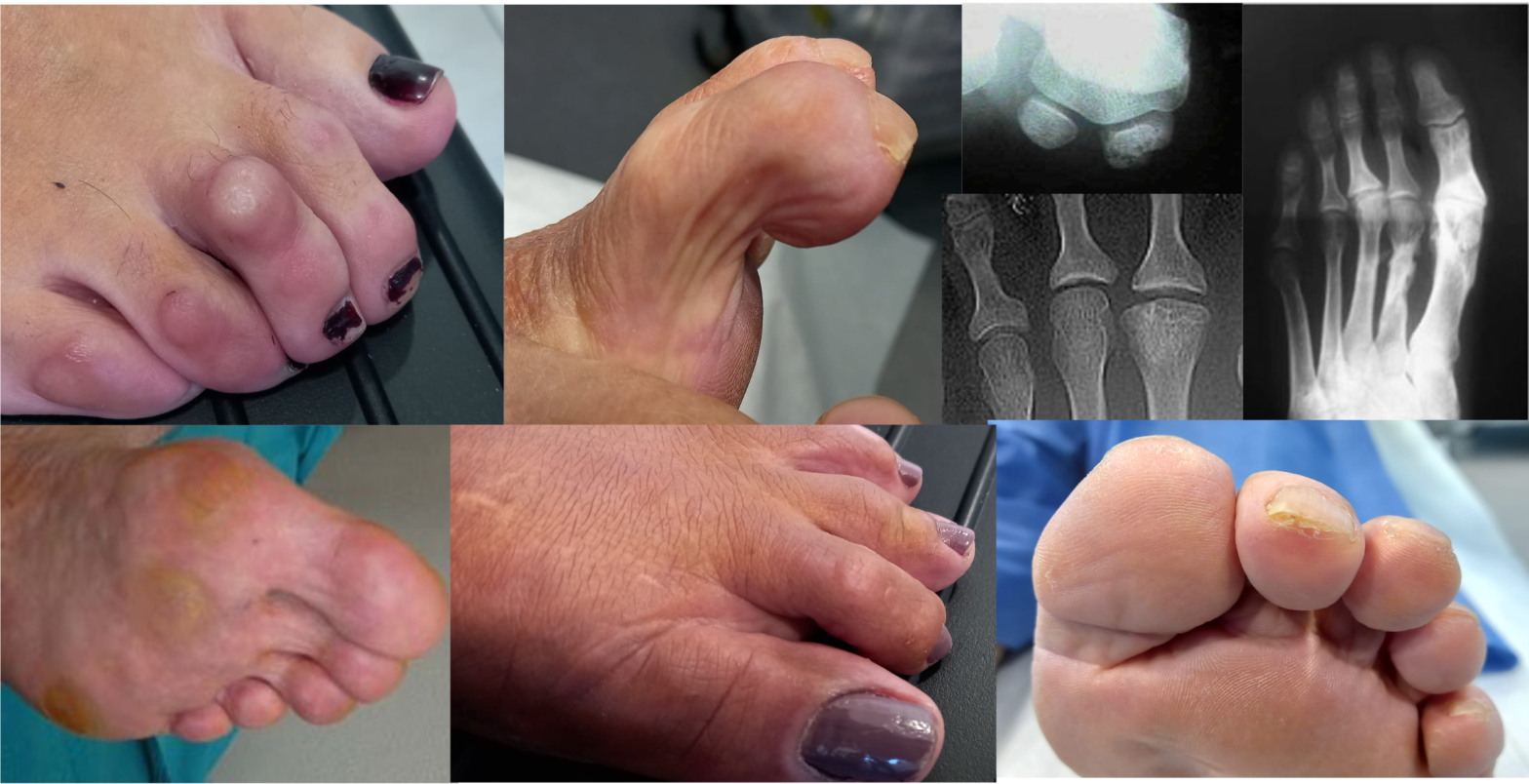
DEDO EN GARRA, DEDO EN MARTILLO, DEDO EN MAZA, METATARSALGIA. NO TODO ES LO MISMO (PARTE 3)
02 diciembre 2021
Dedo en garra, dedo en martillo, dedo en maza, metatarsalgia y otras afecciones del antepie no son lo mismo. Estas dolencias pueden coexistir formando lo que se denomina el pie triangular. Explicamos que es cada una y cómo podemos diagnosticarlo y tratarlo.
DEDO EN GARRA, MARTILLO Y EN MAZO
¿QUÉ ES EL DEDO EN GARRA, MARTILLO O EN MAZA?
Son deformidades de los dedos de los pies que generan dolor y limitación en el uso del calzado, generan con el roce clavos y callosidades de los dedos. Se diferencian en su angulación de las articulaciones:- Dedo en martillo: es la flexión de la articulación interfalángica proximal e hiperextensión de la interfalángica distal.
- Dedo en garra: flexión articulación interfalángica proximal y distal.
- Dedo en maza: extensión de articulación interfalángica proximal y flexión de la distal.
¿QUÉ FACTORES PREDISPONEN EN TENER DEFORMIDAD EN LOS DEDOS?
Hay diferentes factores que afectan a la formación de estas deformidades de los dedos del pie como son:- Factores genéticos o congénitos
- Tipo de calzado: zapatos cortos o con mucho tacón.
- Pies cavos
- Enfermedades reumáticas: artritis reumatoide y psoriasica
- Por cirugías de juanete previas
¿QUÉ SÍNTOMAS PROVOCAN LOS DEDOS EN GARRA, MARTILLO O MAZA?
Esta deformidad de los dedos del pie generan callosidades o clavos y dolor por el hiperapoyo del metatarsiano lo que se denomina metatarsalgia.¿CÓMO TRATAMOS ESTA DOLENCIA?
En primer momento debemos comenzar con un tratamiento conservador adaptando el zapato a ser más cómodo y ancho. Pueden usarse también plantillas o protectores de las callosidades. Si todo esto fracasa el tratamiento quirúrgico es la elección son las artroplastias tipo Duvries o la artrodesis interfalangica proximal .METATARSALGIA
Dolor localizado en la zona de apoyo de los metatarsiano del pie.PATOLOGÍAS QUE CAUSAN METATARSALGIAS
- Hallux valgus y rigidus (puede leer sobre ello en el link https://traumatologosalamanca.com/traumatologia-cirugia-ortopedica/hallux-rigidus-juanete-de-sastre-helomas-o-clavos/)
- Alteración de los huesos sesamoideos.
- Metatarsalgia mecánica o de apoyo
- Fractura de fatiga del cuello metatarsiano
- Enfermedad de Freiberg (Köhler II)
- Neuroma de Morton (puede leer sobre ello en el link https://traumatologosalamanca.com/traumatologia-cirugia-ortopedica/neuroma-de-morton/)
METATARSALGIA POR ALTERACION DE LOS SESAMOIDEOS
Los sesamoideos pueden generar metatarsalgia o dolor en la planta por diferentes causas a nivel del 1º dedo del pie. Las causas pueden ser por sesamoiditis de sobrecarga, fracturas de estrés y necrosis avascular (Enfermedad de Renander). El paciente presenta dolor en la planta del primer dedo , dificultad para caminar e hiperqueratosis de la planta. Podemos diagnosticarlo por la exploración y complementar el estudio con radiografía y resonancia. Podemos tratarlos conservadoramente con reposo , analgésico o plantillas de descarga. Si no mejora la cirugía puede ayudar pero los resultados suele ser muy variable.METATARSALGIA MECÁNICA O DE APOYO
Se produce por un hiperapoyo de los metatarsianos centrales durante la deambulación en el momento de apoyo del antepie. Esto se produce por aumento de longitud o flexión de algún metatarsiano o desplazamiento de la almohadilla plantar El paciente presenta dolor en la planta al caminar e hiperqueratosis (callos) El diagnostico es por la historia clínica y la exploración pudiendo ayudar la radiografía para ver la estructura ósea del pie. Pueden clasificarse en dos tipos de metatarsalgia, estática o propulsiva variando la causa y por tanto la forma de la hiperqueratosis o callo en la planta. El tratamiento consiste en normalizar las presiones de los metatarsianos en el apoyo de la marcha. Esto podemos lograrlo con plantillas o cambios de calzado con suela rígida conformada. Y si falla el tratamiento conservador la cirugía puede ayudarnos como la osteotomía de Weil. (puede apreciar la osteotomía de weil en la parte final del video https://www.youtube.com/watch?v=GajyueD1Dog&t=6s)METATARSALGIA POR FRACTURA POR FATIGA DEL CUELLO
Son fracturas que se producen en los metatarsianos por sobrecargas repetitivas . El hueso más afectado es el 2º metatarsiano (Deutschländer). Los pacientes refieren ejercicios intensos previos y repetitivos , siendo frecuentes en deportistas esta lesión. El dolor al deambular e inflamación en el dorso del pie suele ser la clínica de esta lesión. Lo diagnosticamos con un radiografía, en la que se aprecia en ocasiones callos óseo en fase de consolidación o fisura. Si no vemos nada en la radiografía, debemos solicitar RMN o gammagrafía para confirmar el diagnóstico. Su tratamiento es el reposo y la inmovilizaciónMETATARSALGIA EN LA ENFERMEDAD DE FREIBERG (KÖHLER II)
Es la osteonecrosis de la cabeza del 2º metatarsiano. Es más frecuente en mujeres que en hombres (5 a 1). Suele aparecer entre los 15 y 21 años. Se produce por la isquemia vascular del hueso , pero la causa no es bien conocida. La clínica de paciente es dolor al deambular. Y la diagnosticamos con una radiografía simple. El tratamiento conservador es con calzado con suela rígida conformada y plantillas. Si este falla el tratamiento quirúrgico puede ayudarnos. Suele ser limpieza articular , osteotomía o artroplastia de resección.SI TE DUELEN LOS PIES, CONSULTENOS CUIDAMOS TUS PIES CUIDAMOS DE TI.
#dedoengarra #dedoenmartillo #dedoenmaza #callos #clavo #metatarsalgia #operacióndepie #cirugiadepie #dolordepie #nopuedocaminar #traumatólogo #traumatología #Salamanca #ZamoraBIBLIOGRAFIA
- Kim HJ, Suh DH, Yang JH, Lee JW, Kim HJ, Ahn HS, Han SW, Choi GW. Total ankle arthroplasty versus ankle arthrodesis for the treatment of end-stage ankle arthritis: a meta-analysis of comparativestudies. Int Orthop. 2017 Jan;41(1):101-109.
- Xu Y, Zhu Y, Xu XY. Ankle joint distraction arthroplasty for severe ankle arthritis. BMC Musculoskelet Disord. 2017 Feb 28;18(1):96.
- Bernstein M, Reidler J, Fragomen A, Rozbruch SR. Ankle Distraction Arthroplasty: Indications, Technique, and Outcomes. J Am Acad Orthop Surg. 2017 Feb;25(2):89-99.
- Henbühl N, Zwicky L, Bolliger L, Schädelin S, Hintermann B, Knupp M. Mid- to Long-term Results of Supramalleolar Osteotomy. Foot Ankle Int. 2017 Feb;38(2):124-132.
- Hintermann B, Knupp M, Barj A. Supramalleolar Osteotomies for the Treatment of Ankle Arthritis J Am Acad Orthop Surg 2016;24: 424-432.
- Thevendran G, Shah K, Pinney SJ, Younger AS. Perceived risk factors for nonunion following foot and ankle arthrodesis. J Orthop Surg (Hong Kong). 2017 Jan;25(1):2309499017692703.
- Van der Plaat LW, Van Engelen SJ, Wajer QE, Hendrickx RP, Doets KH, Houdijk H, van Dijk CN. Hind- and Midfoot Motion After Ankle Arthrodesis. Foot Ankle Int. 2015 Dec;36(12):1430-7.
- Roukis TS, Elliott AD. Incidence of revision after primary implantation of the Salto ® mobile version and Salto Talaris ™ total ankle prostheses: a systematic review. J Foot Ankle Surg. 2015 May- Jun;54(3):311-9.
- Daniels TR, Mayich DJ, Penner MJ. Intermediate to Long-Term Outcomes of Total Ankle Replacement with the Scandinavian Total Ankle Replacement (STAR). J Bone Joint Surg Am. 2015 Jun 3;97(11):895-903.
- Lefrancois T, Younger A, Wing K, Penner MJ, Dryden P, Wong H, Daniels T, Glazebrook M. A Prospective Study of Four Total Ankle Arthroplasty Implants by Non-Designer Investigators. J Bone Joint Surg Am. 2017 Feb 15;99(4):342-348.
- Stavrakis AI, SooHoo NF. Trends in Complication Rates Following Ankle Arthrodesis and Total Ankle Replacement. J Bone Joint Surg Am. 2016 Sep 7;98(17):1453-8.
Dr. David Pescador

Dr. David Pescador
TraumatólogoEl Dr. David Pescador es especialista en Traumatología y Cirugía Ortopédica, con subespecialidad en Cirugía de Columna Vertebral.
